Genital papillomvirus-infektion
Huvudartikel
Till innehållsförteckningen för Referensmetodik: Sexuellt överförbara infektioner (STI)
Genital papillomvirus-infektion (A63.0)[redigera]
Etiologi[redigera]
Humana papillomvirus (HPV), elementkod MSHD10213
Smittämnet[redigera]
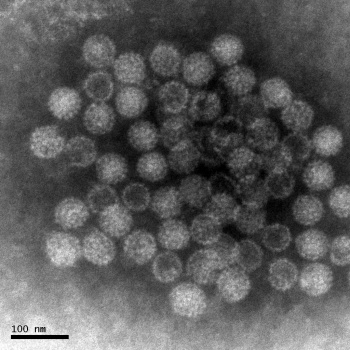
Humana papillomvirus är små, stabila, icke-höljebärande DNA-virus inom familjen Papillomaviridae. Genomet är en dubbelsträngad cirkulär DNA-molekyl som är uppbyggd av cirka 7.900 nukleotider. All kodande information är lagrad på en av DNA-strängarna. Sex tidiga gener, El, E2 och E4-E7, kodar för regler- och replikationsfunktioner och två sena gener, L1 och L2, kodar för viruskapsidbyggstenar.
Hittills har 113 humana papillomvirustyper identifierats och fullständigt sekvensbestämts. Dessutom föreligger ytterligare ett hundratal identifierade men ännu inte klassificerade papillomvirussekvenser. De olika typerna kan klassificeras i olika genetiskt besläktade species. Typer inom samma species har påtagliga likheter beträffande sin tropism (hud eller slemhinna), väsentlig överföringsväg (indirekt kontaktsmitta eller sexuellt överförda) samt vilka sjukdomar de orsakar och deras onkogena potential (vårtor, kondylom eller cancer).
HPV-typer som infekterar huden[redigera]
Flertalet kutanta HPV-infektioner är helt asymtomatiska. För etablering av infektion krävs att virus infekterar delande celler i basalcellslagret. I synnerhet de virus som orsakar vårtor sprids lättare till skadat epitel som t.ex. hudsprickor vid handbollsspel eller uppblött epitel i simhallar. En stor grupp virus, som vanligen ger asymtomatiska infektioner, kan dock nå basalcellslagret i intakt hud via hårsäckar. HPV-typ 1 är den dominerande orsaken till fotvårtor, medan HPV typ 2 är den vanligaste orsaken till hudvårtor på andra ställen på kroppen.
HPV-typer som infekterar slemhinnor[redigera]
Dessa virus indelas i två kategorier, lågrisktyper och högrisktyper, med avseende på samband med malignitet. Lågrisktyperna som orsakar kondylom (könsvårtor) är sinsemellan nära besläktade, HPV-typerna i species A6 i synnerhet HPV 6 och 11 är dominerande orsak till kondylom.
Högrisktyperna som orsakar cancer finns huvudsakligen i 2 sinsemellan avlägset besläktade grupper: HPV 16 och dess släktingar HPV 35, 31, 33,58 och 52 i species A9 samt HPV 18 och dess släktingar HPV45 och 68 i species A7. HPV 16 är den dominerande orsaken till cervixcancer och andra HPV-orsakade cancerformer. HPV16s släktingar i species A9 kan också orsaka cervixcancer, men inte med lika hög risk som HPV16. HPV18 och dess släktingar orsakar i synnerhet adenocarcinom i cervix, medan HPV16 och A9-species i första hand orsakar skivepitelcancer.
Klinik[redigera]
Kutana HPV kan orsaka vårtor på huden. Det finns ännu inte ett enda fall beskrivet av malignifiering av sådana varför hudvårtor är ett begränsat medicinskt problem.
Hudcancer är HPV-associerad hos patienter med den mycket sällsynta immunbristsjukdomen epidermodysplasia verruciformis. En tredjedel av dessa patienter får skivepitelcancer på solbelyst hud. I lesionerna påvisas HPV 5 eller HPV 8. HPV kan även påvisas i hudcancer som uppstår hos njurtransplanterade som står på livslång immunsuppression.
Kondylom (sexuellt överförda s.k. könsvårtor) återfinns i larynx, i munhålan och anogenitalt. Respiratorisk papillomatos innebär kondylom i luftvägarna. Detta är en mycket sällsynt sjukdom, men den är av medicinsk betydelse eftersom stämbanden engageras och sjukdomen har ett recidiverande, progredierande förlopp som allvarligt kan hota andningen. Anogenitala kondylom är mycket vanliga. Årlig incidens i Sverige är uppskattad till cirka 40000 behandlingskrävande fall, Kondylom innebär därför ett påtagligt medicinskt problem av både somatisk och psykosocial natur.
Kondylom läker ofta spontant utan terapi men det är inte ovanligt med långvariga problem i form av förhårdnader och smärtsamma fissurer. Recidiv efter behandling är vanligt. I enstaka fall kan malignifiering förekomma. Så kallade Buschke-Löwenstein-tumörer eller jättekondylom är maligna tumörer som uppstår ur ohämmat tillväxande kondylom.
Både cervikal skivepitelcancer och adenocarcinom i cervix uteri hos kvinnor och analcancer är regelmässigt orsakade av högrisk HPV, vanligen HPV16. Vulvacancer är HPV-orsakad i cirka 30 % av fallen. Vaginalcancer, peniscancer och tonsillcancer är HPV-orsakade i cirka 50 % av fallen. HPV-associerad tonsillcancer skiljer sig från HPV-negativ tonsillcancer genom att inte ha rökning och alkoholkonsumtion som riskfaktor, men förekommer företrädesvis hos yngre och har munsex som riskfaktor. HPV-associerad tonsillcancer är mer känslig för radioterapi än den HPV-negativa formen. Incidensen av HPV-positiv tonsillcancer är i stigande, medan incidensen för HPV-negativ tonsillcancer förefaller att minska.
Cervixcancer hos kvinnor förekommer över hela jorden men den geografiska fördelningen är mycket ojämn. I vissa delar av latinamerika och Afrika söder om Sahara förekommer livstidsrisker för cervixcancer på uppemot 10 %. De lägsta cervixcancertalen förekommer i Kuwait samt hos ortodoxa judar i Israel. Livstidsrisken för cervixcancer i Sverige var cirka 2 % innan införande av det allmänna gynekologiska cellprovtagningsprogrammet och har idag sjunkit till cirka 0,5 %.
Skillnaden i förekomst av cervixcancer kan till allra största delen förklaras med skillnader i sexualvanor, med medianantalet sexualpartner över livstiden hos männen som den viktigaste faktorn. Väl organiserade screeningprogram förklarar den ytterligare skillnad i förekomst som ses.
Det finns otvetydiga både experimentella och epidemiologiska belägg för att högriskpapillomvirustyper orsakar invasiv cervixcancer. Nästan samtliga fall av cervixcancer innehåller någon typ av HPV. I samtliga cellinjer som har etablerats från kvinnor med cervixcancer kan HPV påvisas, även om cellinjerna odlats in vitro under lång tid. Papillomvirusgenomet kodar för två tidiga genomprodukter, E6 och E7, som förmår immortalisera keratinocyter. E6 binder till p53-proteinet och aktiverar ett p53-specifikt proteas som bryter ned detta. I cervixcancer ser man vanligen en icke-muterad p53 gen samt transkription av p53, men inget p53 protein kan påvisas. E7 binder till Rb och inaktiverar den funktionellt genom att förhindra att transkriptionsfaktorn E2F binder till Rb. Genomet innehåller också en genprodukt E2, som utövar en kontroll av expressionen av E6 och E7.
Vid invasiv cancer återfinns HPV -genomet oftare integrerat i det mänskliga genomet än episomalt. Integrationsstället drabbar regelmässigt E2-regionen så att dess roll som repressivt element med effekt på E6 och E7 avblockeras.
Epidemiologi[redigera]
Epidemiologi beskrivs ovan under klinik.
Provtagning[redigera]
Följ länken för detaljerad information
Laboratoriediagnostik[redigera]
Följ länken för detaljerad information. Identifiering och klassificering av humana papillomvirus bygger på molekylärbiologisk metodik.
Mikrobiologisk diagnostik av HPV–infektion är känsligare än cytologisk diagnostik avseende förekomst av förstadier till cervixcancer. I Sverige rekommenderas HPV-diagnostik av Svensk Förening för Obstetrik och Gynekologi som ett diagnostiskt hjälpmedel vid fynd av lätt cellförändring eller eljest oklar cytologi. Eftersom nästan samtliga cervixcancrar är HPV-associerade behöver HPV-negativa cytologiska fynd inte närmare utredas. Användning av HPV-test som kontroll efter behandling rekommenderas för att förutsäga recidivrisk. I synnerhet i USA används HPV-test som ett primärt screeningtest i stället för cytologi. Även om testet är mera känsligt, så har det lägre specificietet än cytologi och om och hur HPV-test kan komma att användas inom allmän screening i Sverige är ännu oklart.
Behandling[redigera]
Det finns ännu ingen specifik antiviral behandling. Mot vårtor används olika former av destruktiva eller cytolytiska behandlingar. Mot kondylom kan antingen ett cytotoxiskt medel (podofyllotoxin), ett immunstimulernade medel (imikvimod), kirurgi, frysning eller bränning användas. HPV-orsakade cellförändringar behandlas vanligen kirurgiskt, men frysning och bränning förekommer också.
Prevention[redigera]
Vaccination med virus-lika partiklar är godkänt i Sverige sedan 2006. Dessa vaccin ger ett huvudsakligen typ-specifikt skydd, dvs de fungerar i huvudsak endast mot de virus som finns i vaccinet. I Sverige finns idag två vacciner godkända, ett mot HPV16 och 18 samt ett mot HPV6, 11, 16 och 18. Bägge skyddar bra mot infektion med de viktigaste cancerframkallande HPV-typerna. Kondylom och respiratorisk papillomatos som orsakas av HPV6 eller 11 förebyggs dock endast om vaccinet innehåller HPV6 /11. Vaccination har ingen terapeutisk effekt för redan infekterad individ och det är därför viktigt att vaccination ges tidigt i livet- bäst effekt nås om de ges före eller strax efter sexualdebuten. Socialstyrelsen har föreslagit allmän vaccination av 11-12-åriga flickor i skolan i Sverige och vaccination av flickor i åldrarna 13-17 år ingår i läkemedelsförmånen.
REFERENSER[redigera]
- 1. Swedish National Board of Health and Welfare. Background to a vaccination program against Human Papillomavirus in Sweden. SoS-rapport 2008.
- 2. Arbyn, M., Dillner, J., Schenck, U., Nieminen, P., Weiderpass, E., Da Silva, J.D., Jordan, J., Ronco, G., McGoogan, E., Patnick, J., Sparen, P., Herbert, A. and Bergeron, C. Methods for screening and diagnosis. In: “European guidelines for quality assurance in cervical cancer screening - Second edition”. Luxembourg: Office for Official Publications of the European Communities. Kapitel 3, 69-152. 2008.
- 3. Dillner, J., Arbyn, M. and Dillner, L. Monitoring of Human Papillomavirus vaccination. Clinical and Experimental Immunology. 2007; 148:199-207.
- 4. Bistoletti, P., Ellström, A., Dillner, J., Sennfält, K., Sparén, P. and Strander, B. Cervix cancer screening can be cost-effective. Combination of vaginal smears and the HPV test should be even more beneficial. Läkartidningen 2005; 24:1874-1879.
- 5. Arbyn, M., Sasieni, P., Meijer, C.J., Clavel, C., Koliopoulos, G. and Dillner, J. Clinical applications of HPV testing: A summary of meta-analyses. Vaccine. 2006; 24 (Suppl 3):S78-89.