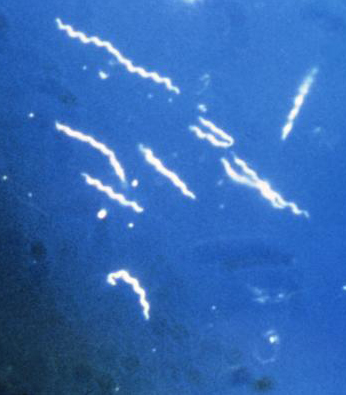
Borrelia
Huvudartikel
Till innehållsförteckningen för Referensmetodik: Infektioner i centrala nervsystemet
Borrelia, Lyme disease[redigera]
Smittämnet[redigera]
Lyme borrelios (Lyme disease) orsakas av Borrelia burgdorferi, tillhörande genus Borrelia inom ordningen Spirochaetales. Bakterierna är rörliga 4-30 µm långa och 0,2-0,3 µm tjocka gramnegativa, flagellförsedda spiroketer. Fyra species har beskrivits, B. burgdorferi sensu stricto, B. garinii, B. afzelii och B. japonica. De tre första har påvisats vid humaninfektion. B. garinii har framför allt associerats till neurologiska manifestationer. Ytterligare genotyper kan finnas i Europa. B. burgdorferi överförs med fästingbett och reservoar för spiroketen är värddjur för fästingar, framför allt smågnagare.
Patogenes[redigera]
Sjukdomsbild[redigera]
B. burgdorferi kan sprida sig lokalt i huden och inom dagar till veckor ge upphov till en expanderande hudrodnad eller ring på platsen för ett fästingbett, erythema migrans. Mindre vanliga hudmanifestationer är borrelialymfocytom, en blåröd svullnad av örsnibb eller mamill, och akrodermatit, en blåröd missfärgning och atrofi av huden, oftast på fötter eller händer. Spiroketerna kan även sprida sig via blodbanan och ge upphov till sekundära huderytem eller symtom från andra organ, vanligen nervsystem och leder, mer sällan från hjärtat. Vid hjärtpåverkan ses bradyarytmi med AV-block, vid artrit recidiverande ledsvullnad, ofta i större leder såsom knälederna.
Infektion i nervsystemet kan ge symtom på kronisk meningit (trötthet, nackstelhet, intermittent huvudvärk, illamående och subfebrilitet), ibland förenat med migrerande muskelsmärtor, radikulitsmärtor, sensibilitetsrubbning eller pareser, vanligen facialispares. Akut meningit kan också förekomma. Ca 5-20 % av fall med facialpares hos vuxna och upp till 50 % hos barn orsakas under sen- sommar och höst av borrelia.
Borreliainfektion är ofta asymtomatisk och läker som regel utan behandling även vid symtomgivande infektion. I ett mindre antal fall ses en kronisk, progredierande sjukdomsbild med symtom från hud, nervsystem eller leder. Antibiotikabehandling ger som regel symtomfrihet, men läkningsförloppet kan vara långdraget och resttillstånd förekommer.
Epidemiologi (uppdaterad mars 2012)[redigera]
Borrelia är en vektorburen zoonos som sprids via fästingar av släktet Ixodes. I Sverige orsakas infektionen huvudsakligen av arterna B. afzelii, B. garinii och mer ovanligt B. burgdorferi sensu stricto. I Sverige förkommer idag borreliainfektioner i större delen av landet men främst i landets södra och mellersta delar och längs Östersjöns och Bottenhavets kuster. Risk för smitta efter ett fästingbett uppskattas till 1/150 bett, baserat på epidemiologiska studier i södra Sverige. Borrelia är inte anmälningspliktigt i Sverige och det är därför svårt att avgöra hur hög incidensen är. Med hjälp av resultaten från en studie från 1995 som utfördes i södra delen av landet uppskattades antalet fall i Sverige ligga mellan 5 000 och 10 000 per år. Men eftersom fästingarna ökat i antal de senaste decennierna, så har sannolikt även antalet fall ökat sen dess.
Prevention[redigera]
Inget fungerande vaccin finns tillgängligt.
För övrigt gäller att följa råd om hur man bäst skyddar sig mot fästingbett och om hur man tar bort fästingar. Myggmedel saknar effekt mot fästingbett.
Provtagning[redigera]
Laboratoriediagnostik[redigera]
Allmänt[redigera]
Flera metoder finns beskrivna för diagnostik av borreliainfektion. Diagnosen erytema migrans ställs i första hand utifrån typisk klinisk bild. Laboratoriediagnostik rekommenderas i första hand vid misstanke om borreliainfektion med multipla erytem eller andra hudmanifestationer, infektion som drabbar andra organsystem, exempelvis leder, hjärta eller centrala nervsystemet. Den baseras huvudsakligen på serologi med antikroppsdetektion i serum och cerebrospinalvätska (Csv). Serologisk undersökning kan visserligen konfirmera infektion men inte om infektionen pågår, eftersom aktivitetsmarkörer i olika skeden av infektionen saknas. Immunblottester (Western blot) baserade på rekombinanta antigen kan komplettera serologisk analys, och kan teoretiskt skilja tidigt och sent immunsvar, men kan inte heller avgöra om infektionen pågår. Ett annat problem med serologiska undersökningar är att primär kalibrator saknas, vilket bidrar till svårigheter att definiera specificitet för olika kommersiella tester. Tillgänglig alternativ diagnostik har ofta låg sensitivitet eller är otillräckligt utvärderad. Det senare gäller så kallade lymfocyttransformations-tester, som för närvarande inte officiellt rekommenderas. Bland alternativa validerade metoder kan nämnas nukleinsyraamplifiering (PCR) som har skiftande och för flera provtyper låg känslighet. PCR erbjuds på några svenska laboratorier. Odling används inte rutinmässigt i landet, men kan utföras på Csv, blod och ledvätska. Odling av blod, men verifiering av odlingsfynd med PCR, är tämligen känslig vid multipla erytem.
Referensmetodik[redigera]
Serologi[redigera]
Serum och Csv analyseras avseende förekomst av specifika antikroppar mot Borrelia och tecken på intratekal antikroppsproduktion. ELISA torde vara den bästa metoden för standardisering och hantering av stora provserier. Antigen vid ELISA kan utgöras av helcellssonikat av odlade spiroketer, fraktioner av sonikat och ultracentrifugat (ex flagell), eller rekombinantantigen. ELISA baserad på renade antigen eller rekombinantantigen har visat bättre sensitivitet/specificitet än helcellssonikat som innehåller fler korsreagerande antigen. Det är oklart hur mycket olika serotyper eller isolat från olika geografiska regioner påverkar utfallet av serologisk diagnostik. Flera kommersiella EIA-kit, baserade på olika antigen, finns tillgängliga. Av dessa har framför allt ett flagellbaserat kit (DAKO) använts vid svenska laboratorier, i vissa fall som komplement till egentillverkat sonikatantigen.
Falskt positiva test ses med sera från syfilispatienter. Captureteknik förbättrar IgM-diagnostiken och underlättar påvisande av intratekal antikroppsproduktion vid samtidig analys av serum och cerebrospinalvätska. Falskt positiva IgM-test för Borrelia förekommer vid t ex EBV- och CMV-infektion samt vid autoimmuna tillstånd. Borreliasera kan ge positiv reaktion med FTA-abs men är negativa i syfilisspecifika test som TPHA.
Med tillgängliga metoder kan specifika antikroppar påvisas i serum i 10-50 % vid erythema migrans (högre frekvens vid multipla erytem), i 60-70 % vid lymfocytom eller hjärtpåverkan, och i närmare 100 % vid akrodermatit eller artrit. Vid neuroborrelios kan antikroppar påvisas i serum i 30-50 % efter 2 veckors sjukdomsduration och i närmare 100 % efter 6-8 veckor. Antikroppar ses ofta tidigare i cerebrospinalvätska än i serum, och intratekal antikroppsproduktion kan påvisas i upp till 80 % efter 2 veckors neurologisk sjukdom.
Övriga diagnostiska metoder[redigera]
Odling[redigera]
Bakterieisolering ger positivt utbyte i 50-90 % av biopsier från hudmanifestationer och i 10-20 % från cerebrospinalvätska vid neuroborrelios. Enstaka isolat finns beskrivna från blod, ledvätska och organbiopsier. Odling är olämplig för rutindiagnostik pga dåligt utbyte (med undantag för hudmanifestationer), kostsamt odlingsmedium och lång odlingstid (flera veckor). Odling sker i Kellys modified medium, ett lösligt medium som inkuberas i 35 °C. Ev spiroketer identifieras i mörkfältsmikroskop.
Antigendetektion[redigera]
Antigenpåvisning i biopsier med färgning eller med antikroppar har begränsat värde pga av den låga bakterieförekomsten i infekterad vävnad. Antigenpåvisning i urin med hjälp av antikroppar har visat goda resultat i djurförsök men fungerat mindre väl för humanmaterial.
Nukleinsyrapåvisning[redigera]
PCR har i jämförande studier givit motsvarande, eller något bättre, utbyte än odling från hudbiopsier, cerebrospinalvätska och blod, och har givit positivt resultat i urin i över 50 % vid neuroborrelios. Positiva PCR-resultat har även rapporterats i urin från symtomfria personer med positiv borreliaserologi. Vid artrit, där odling nästan undantagslöst är negativ, kan plasmidbundna DNA-sekvenser påvisas med PCR i mycket hög frekvens, medan kromosombundna sekvenser påvisas mindre ofta. Metoden kan inte anses tillräckligt utvärderad för rutindiagnostik.
Övrig serologi[redigera]
Antikroppspåvisning med immunfluorescens kan användas som alternativ till ELISA, men är svårare att standardisera och har i jämförande studier visat sämre sensitivitet/specificitet än ELISA. Med Western blot (Wb) kan antikroppar påvisas tidigare i sjukdomsförloppet än med ELISA, men då med sämre specificitet. Med krav på ett flertal band i Wb kan hög specificitet erhållas, men sensitiviteten går då förlorad vid diagnostik av tidiga sjukdomsfall. Svårigheter att standardisera metoden gör den mindre lämplig för rutindiagnostik. Wb finns tillgänglig i kommersiella kit. Värdet av Wb som “konfirmerande” test är begränsat eftersom påvisande av antikroppar inte är liktydigt med aktuell infektion och negativa antikroppstest är vanligt förekommande vid kort sjukdomsduration.
Tillämpning och tolkning av borreliaserologi[redigera]
Erythema migrans är i första hand en klinisk diagnos och serologisk provtagning är i flertalet fall ej motiverad. Övriga kliniska manifestationer motiverar serologisk provtagning och vid misstanke om neuroborrelios bör lumbalpunktion utföras.
IgM-antikroppar mot Borrelia i serum talar för en aktuell infektion, framför allt vid påvisad titerstegring eller vid samtidig titerstegring eller förekomst av IgG-antikroppar. Falskt positiva IgM-reaktioner förekommer dock, och vid misstanke om neuroborrelios väger de kliniska sjukdomstecknen samt likvorfynd tungt vid bedömning av de serologiska fynden. Vid serologisk undersökning analyseras alltid IgM- och IgG-antikroppar samtidigt. Vid misstanke om neuroborrelios analyseras serum och cerebrospinalvätska tagna vid samma tillfälle. Intratekal antikroppsproduktion påvisas med samtidig undersökning av serum och likvor med captureteknik, alternativt med ett titerindex. Påvisande av specifik intratekal antikroppsproduktion talar mycket starkt för aktuell neuroborrelios, framför allt vid samtidig cellstegring i likvor. En isolerad IgG-stegring i serum kan bero på en aktuell infektion som pågått längre tid (månader), men kan även stå kvar efter en tidigare klinisk eller subklinisk infektion. I fall med kort anamnes på neuroborrelios (mindre än två veckor) kan antikroppstest utfalla negativt i både serum och likvor, trots typisk sjukdomsbild, pleocytos och positiv odling i cerebrospinalvätska.
Förnyad serologi visar ibland titerstegring för IgM och IgG efter ett par veckor, även om antibiotikabehandling givits. Hos patienter med facialispares utan klinisk misstanke på borreliainfektion kan man avstå från lumbalpunktion men ta serologiprov, och upprepa detta efter 2-3 veckor om första provet utfaller negativt.
Höga antikroppstitrar i serum av både IgM- och IgG-klass, sjunker som regel långsamt inom de närmaste månaderna efter antibiotikabehandling, men kan kvarstå höga mer än ett år, framför allt avseende IgG. Intratekal antikroppsproduktion kan kvarstå flera år efter behandling och kliniskt utläkt neuroborrelios. Upprepad provtagning efter behandling behöver ej göras rutinmässigt.
Förekomst av IgG-antikroppar har ofta låg specificitet för aktuell behandlingskrävande infektion i områden med hög seroprovalens (25 % av befolkningen i vissa områden). Upprepad provtagning, med minst ett par veckors intervall kan ge vägledning vid diagnostik av kliniskt oklara fall. Hos patienter med diffusa symtom som t ex trötthet och huvudvärk i mer än två månader torde en negativ serologi utesluta neuroborrelios och lumbalpunktion behöver ej utföras. Vid liknande symtombild och
positiv serologi torde kronisk neuroborrelios uteslutas av normal cerebrospinalvätska och avsaknad av intratekal antikroppsproduktion.
Referensstammar[redigera]
- B. burgdorferi ATCC 35210
Svarsrutiner[redigera]
Laboratorierapportering[redigera]
Referensfunktioner[redigera]
Borrelia rapporteras ej.
Referensfunktioner[redigera]
REFERENSER[redigera]
- Baranton G, Postic D, Saint Giron 1, Boerlin P, Piffaretti J-C, Assous M, Grimont PAD. Delineation of Borrelia burgdorferi sensu stricto, Borrelia garinii sp. nov. and group VS461 associated with Lyme borreliosis. Int J Syst Bacteriol 1992;42:378-383.
- Bunikis J, Olsen B, Westman G, Bergström S. Variable serum immunoglobulin responses against Borrelia burgdorferi sensu lato species in a population at risk for and patients with Lyme disease. J Clin Microbiol 1995;33: 1473-1478.
- Christen HJ, Eiffert H, Ohlenbusch A, Hanefeld F. Evaluation of the polymerase chain reaction for the detection of Borrelia burgdorferi in cerebrospinal fluid of children with acute peripheral facial palsy. Eur J Pediatr 1995; 154:374-377.
- Dressler F, Whalen JA, Reinhardt BN, Steere AC. Western blotting in the serodiagnosis of Lyme disease. J Infect Dis 1993;167:392-400.
- Gerber MA, Shapiro ED, Bell GL, Samieri A, Padula SJ. Recombinant outer surface protein C ELISA for the diagnosis of early Lyme disease. J Infect Dis 1995;l71:724-727.
- Grodzicki RL, Steere AC. Comparison of immunoblotting and indirect enzyme-linked immunosorbent assay using different antigen preparations for diagnosing early Lyme disease. J Infect Dis 1988;157:790-797.
- Hammers-Berggren S, Hansen K, Lebech A-M, Karlsson M. Borrelia burgdorferi-specific intrathecal antibodyproduction in neuroborreliosis: a follow-up study. Neurol 1993;43:169-
- Hammers-Berggren S, lebech A-M, Karlsson M, Svenungsson B, Hansen K, Stiernstedt G. Serological follow-up after treatment of erythema migrans and neuroborreliosis. J Clin Microbiol 1994;32: 15 19-1525.
- Hansen K, Hindersson P, Strandberg-Pedersen N. Measurement of antibodies to the Borrelia burgdorferi flagellum improves serodiagnosis in Lyme disease. J Clin Microbiol 1988;26:338-346.
- Hansen K, Lebech A-M. Lyme neuroborreliosis: a new sensitive diagnostic assay for intrathecal synthesis of Borrelia burgdorferi specific immunogiobulin G, A and M. Ann Neurol 1991;30:197-205.
- Hansen K, Pil K, Lebech A-M. Improved immunoglobulin M serodiagnosis in Lyme borreliosis by using a μ-capture enzyme-linked immunosorbent assay with biotinylated Borrelia burgdorferi flagella. J Clin Microbiol l991;29: 166-173.
- Karlsson M, Hovind-Hougen K, Svenungsson B, Stiernstedt G. Cultivation and characterization of spirochetes from cerebrospinal fluid of patients with Lyme borreliosis. J Clin Microbiol 1990;28:473-479.
- Karlsson M, Möllegård 1, Stiernstedt G, Wretlind B. Comparison of Western blot and enzyme-linked immunosorbent assay for diagnosis of Lyme borreliosis. Eur J Clin Microbiol 1989;8:871-877.
- Karlsson M, Stiernstedt G, Granström M, Åsbrink E, Wretlind B. Comparison of flagellum and sonicate antigens for serological diagnosis of Lyme borreliosis. Eur J Clin Microbiol Infect Dis 1990;9: 169-177.
- Lebech A-M, Hansen K. Detection of Borrelia burgdorferi DNA in urine samples and cerebrospinal fluid samples from patients with early and late neuroborreliosis by polymerase chain reaction. J Clin Microbiol 1992;30: 1646-1653.
- Magnarelli LA, Andersson JF, Barbour AG. Enzyme-linked immunosorbent assay for Lyme disease: Reactivity of subunits of Borrelia burgdorferi. J Infect Dis 1989; 159:43-49.
- Magnarelli LA, Andersson JF, Johnson RC, Nadelman RB, Wormser GP. Comparison of different strains of Borrelia burgdorferi sensu lato used as antigens in enzyme-linked immunosorbent assays. J Clin Microbiol 1 994;32: 1154-1158.
- Nocton JJ, DresslerF, Rutledge BJ, Rys PN, Persing DH, Steere AC, Detection of Borrelia burgdorferi DNA by polymerase chain reaction in synovial fluid from patients with Lyme arthritis. N Engl J Med l994;330:229-234.
- Olsson I, von Stedingk L-V, Hanson H-S, von Stedingk K, Åsbrink E, Hovmark A. Comparison of four different serological methods for detection of antibodies to Borrelia burgdorferi in erythema migrans. Acta Derm Venereol 1991;7 1:127-133.
- Steere AC, Grodzicki RL, Craft JE, Shrestha M, Kornblatt AN, Malawista SE. Recovery of Lyme disease spirochetes from patients. Yale J Biol Med 1984;57:557-560.
- Steere AC, Grodzicki RL, Kornblatt AN, Craft JE, Barbour G, Burgdorfer W, Schmidt GP,Johnson E, Malawista SE. The spirochetal etiology of Lyme Disease. N Engl J Med 1983;308:733-740.
- Stiemstedt G. Tick-borne Borrelia infection in Sweden. Scand J Infec Dis Suppl 1985;45:1-70.
- Stiernstedt GT, Granstrom M, Hederstedt B, Skoldenberg B. Diagnosis of spirochetal meningitis by enzyme-linked immunosorbent assay and indirect immunofluorescence assay in serum and cerebrospinal fluid. J Clin Microbiol 1985;21:819-825.
- Van Dam AP, Kuiper H, Vos K, Widjojokusumo A, de JonghBM, Spanjaard L, Ramselaar ACP, Kramer M, Dankert J. Different genospecies of Borrelia burgdorferi are associated with distinct clinical manifestations of Lyme borreliosis. Clin Infect Dis 1993; 17:708-717.
- Wilske B, Preac-Mursic V, Schierz G, Liegi G, Gueye W. Detection of IgM- and IgG antibodies to Borreliaburgdoiferi using different strains and antigens. Zentralbl Bakteriol Hyg Suppl 1989;18:229-309
- Åsbrink E. Cutaneuous manifestations of Lyme borreliosis. Scand J Infect Dis Suppl 199 1:77:44-50.