Trypanosoma cruzi
Huvudartikel, publicerad augusti 2011. Texten är preliminär, ännu ej beslutad genom konsensusförfarande.
Till innehållsförteckning för Referensmetodik:Parasitologisk diagnostik
Trypanosoma cruzi
Smittämne
Trypanosoma cruzi är en protozo som orsakar en vektorburen infektion – amerikansk trypanosomiasis (Chagas sjukdom). T. cruzi är placerad i riskklass 3 av Arbetsmiljöverket (AFS 2005:1), vilket innebär att parasiten orsakar en allvarlig sjukdom med begränsade behandlingsmöjligheter. Mindre däggdjur i människans omgivning är reservoarer. Smittan överförs via blodsugande skinnbaggar (t.ex. Triatoma infestans).
Livscykel
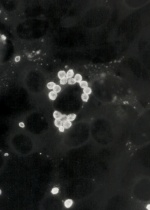
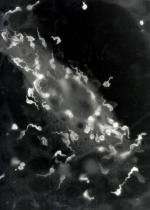
Trypanosoma cruzi har en komplicerad livscykel med olika stadier som utvecklas i humanceller och i insektens tarmkanal. Infektionen överförs via skinnbaggens avföring, där invasiva parasitformer – rörliga, metacykliska trypomastigoter – finns. Skinnbaggarna tömmer tarmen medan de suger blod. Om man därefter kliar sig kan parasiten komma in i det sår som kan uppstå efter bettet. Efter 1–2 veckor ses parasiter i form av trypomastigoter i blodcirkulationen. Trypomastigoter invaderar humanceller, oftast tvärstrimmig och glatt muskulatur samt nervvävnad, där de utvecklas till orörliga amastigoter, delar sig och formar s.k. pseudocystor. Parasiter i pseudocystor utvecklas till rörliga trypomastigoter. Dessa lämnar pseudocystorna och cirkulerar med blodet för att sedan invadera nya celler och forma nya pseudocystor. Ett litet antal trypomastigoter, tillräckligt för att infektera nya skinnbaggar vid blodmål, finns dock kvar i blodcirkulation. Parasiterna utvecklas sedan i insektens tarmkanal till den invasiva formen – metacykliska trypomastigoter. [1]
Symtom och klinisk bild
Sjukdomen karakteriseras av en akut fas som varar upp till 8 veckor och en kronisk fas (efter 8–12 veckor). Vid akut Chagas är de vanligaste symtomen lokal svullnad vid bettet "chagom", feber och trötthet samt svullnad av lymfkörtlar, lever och mjälte; men oftast förblir nyinfekterade patienter asymtomatiska. Skador på hjärtat eller centrala nervsystemet är orsak till akut dödlighet som är cirka 5-10 % (Rassi et al, 2010). Den kroniska fasen är vanligtvis asymtomatisk och kallas för latent fas. Efter flera år kan dock upp till 30 % av personerna i den latenta fasen utveckla obotlig kronisk hjärtmuskelsjukdom eller tarmsjukdom (megaesophagus, megacolon). Kongenital infektion med Chagas sjukdom inträffar när parasiter från en infekterad kvinnas placenta invaderar barnets cirkulation. Av de infekterade barnen är endast 10–30 % symtomatiska, antingen direkt vid födseln eller efter någon månad. Typiska symtom är feber, förstorad lever och mjälte och anemi. Svåra symtom som myokardit, pneumoni och meningoencefalit är mindre vanliga. Av de nyfödda symtomatiska barnen dör 10 % inom 2 dagar.
Epidemiologi
Chagas sjukdom är en zoonos som är endemisk i Central- och Sydamerika. Reservoarer är vilda djur (pungdjur, trögdjur) och husdjur (hund, katt, marsvin). Smittan överförs av skinnbaggar som lever i väggsprickor i primitiva bostäder. Infektionen kan spridas direkt från en person till en annan. Infektionsdosen tros vara låg och inkubationstiden anges till 1–2 veckor. Både antalet kroniska och nya fall har jämte dödligheten minskat i alla endemiska länder under de senaste 20 åren. Man beräknar att cirka 20 % av population i Central- och Sydamerika riskerar infektion. I icke-endemiska områden diagnostiseras Chagas sjukdom hos immigranter och hos personer som har levt i endemiska områden. I Europa finns cirka 30 000 till 40 000 importerade fall, varav de flesta i Spanien. Spridningen av parasiten sker huvudsakligen genom vektorer. Ett antal mindre utbrott i endemiska områden kan kopplas till intag av dryck eller mat kontaminerad med avföring från skinnbaggar. Parasiten kan också överföras från människa till människa via blodtransfusion eller transplantation. Risken för kongenitalinfektion är lika hög (5 %) i endemiska och icke-endemiska områden.
Provtagning och transport
Provmaterial
EDTA- eller kapillärblod
Serum
Provtagning
Laboratoriediagnostik
T. cruzi är placerad i riskklass 3 av Arbetsmiljöverket (AFS 2005:1), vilket innebär att parasiten orsakar en allvarlig sjukdom med begränsade behandlingsmöjligheter. Vid hantering av patientmaterial beaktas skyddsåtgärder lämpliga för användning av biologiska ämnen på skyddsnivå 3, enligt Arbetsmiljöverkets föreskrifter.
Allmänt
Direkt identifiering av parasiter i patientprov är bara lämplig vid diagnostik av akutinfektion. Antalet parasiter i blod vid kronisksjukdom är lågt och infektionen diagnosticeras därför vanligen med indirekta serologiska metoder. Vid misstanke om kongenital infektion hos barn från kvinnor med positiv T. cruzi-serologi tas blodprov för mikroskopi under första levnadsmånaden och prov för serologi vid 6 och 12 månaders ålder.
Referensmetodik
Akut infektion
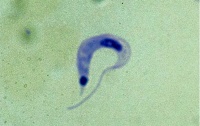
Mikroskopisk påvisning av trypomastigoter i tjock droppe och/eller i tunt utstryk från blod efter Giemsafärgning.
Avläsningskriterier
Trypomastigoter är avlånga, ca 20 µm och har ett vågigt membran och en flagell i främre delen av cellen. En centralt placerad kärna och stor kinetoplast i backre änden färgas violett med Giemsafärg och cytoplasm färgas blå. T. cruzi-trypomastigoter i blodutstryk har oftast ”C” eller ”U”-form. Negativt fynd utesluter inte T. cruzi-infektion.
Förväxlingsorganism
T.rangeli är en apatogen flagellat som förekommer i samma endemiska områden som T. cruzi med vilken den också delar vektorer. Blandade infektioner förekommer både hos vektorer, djur och människor. Trypomastigoter av T. rangeli är smala, avlånga och är större (26-34 µm) än T. cruzi. Kinetoplasten, som är placerad i bakre delen av cellen är liten.
Kvalitetssäkring
T. cruzi trypomastigoter i blodutstryk ingår i UK-NEQAS utskick.
Kronisk infektion
WHO rekommenderar att patientprov testas med minst två olika serologiska tester, t. ex immunofluorescenstest (IF), indirekt hemagglutination eller ELISA. Många standardiserade tester baserade på nativa eller rekombinanta antigener finns på marknaden (se tabell i Lescure et al. 2010). Vid misstanke om kongenital infektion testas för IgG antikroppar vid 6 och 9 månaders ålder. Leishmania-antikroppar och autoantikroppar kan korsreagera med T. cruzi och ge falskt positiva resultat i IF.
Svarsrutiner
Mikroskopi:
Trypomastigoter av T. cruzi påvisade
Inga trypomstigoter påvisade.
Antikroppspåvisning:
Inga antikroppar mot T. cruzi påvisade
Antikroppar mot T. cruzi påvisade
Övriga diagnostiska metoder
- Mikrohematokrit-metod för mikroskopisk påvisning av parasiter i navelsträngsblod eller perifert blod från barn under första månaden efter födseln.
- PCR-baserade metoder för påvisning av parasit-DNA
Laboratorierapportering
Infektion med Trypanosoma cruzi är inte anmälningspliktig.
Litteraturhänvisningar
- Castro E. Chagas disease: lessons from routine donation testing. Transfusion Medicine. 2009;19:16-23.
- Lescure F-X., Le Loup G., Freilij H., Develoux M., Paris L., Brutus L., Pialoux G. Chagas disease: changes in knowledge and management. Lancet Inf. Dis. 2010;10:556-570.
- Rassi A. Jr., Rassi A., Marin-Neto JA. Chagas disease. Lancet. 2010;375:1388-1402.
- Rodrigues Coura J., Borges-Pereira J. Chagas disease: 100 years after its discovery. A systemic review. Acta Tropica. 2010; 115:5-13.