Skillnad mellan versioner av "Schistosoma spp."
| (31 mellanliggande sidversioner av samma användare visas inte) | |||
| Rad 1: | Rad 1: | ||
| − | '''Huvudartikel, publicerad augusti 2011 | + | '''Huvudartikel''', publicerad augusti 2011. |
------- | ------- | ||
''Till innehållsförteckning för [[Referensmetodik:Parasitologisk diagnostik]]'' | ''Till innehållsförteckning för [[Referensmetodik:Parasitologisk diagnostik]]'' | ||
| Rad 5: | Rad 5: | ||
==''Schistosoma'' spp.== | ==''Schistosoma'' spp.== | ||
| − | |||
===Smittämne=== | ===Smittämne=== | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
Human schistosomiasis orsakas av parasitära blodmaskar (trematoder). Parasiten har en infektiös larvform som finns i sötvatten i endemiska områden (t.ex. Malawisjön, Viktoriasjön). De vanligaste arterna är ''Schistosoma mansoni'', ''S. japonicum'' och ''S. hematobium.'' I mindre utsträckning förekommer arterna ''S. intercalatum'' och ''S. mekongi. | Human schistosomiasis orsakas av parasitära blodmaskar (trematoder). Parasiten har en infektiös larvform som finns i sötvatten i endemiska områden (t.ex. Malawisjön, Viktoriasjön). De vanligaste arterna är ''Schistosoma mansoni'', ''S. japonicum'' och ''S. hematobium.'' I mindre utsträckning förekommer arterna ''S. intercalatum'' och ''S. mekongi. | ||
| − | |||
===Livscykel=== | ===Livscykel=== | ||
| − | |||
Parasiten har en invecklad livscykel med människa som värd för hon- och hanmaskar och en sötvattensnäcka som intermediär värd, i vilken det infektiösa larvstadiet utvecklas. Den i vatten fritt levande larvformen av parasiten, cerkarien, attraheras till hud, tränger igenom den och vandrar med cirkulationen till leverns blodkärl. Efter cirka en månad har larverna utvecklas till könsmogna maskar, som producerar hundratals ägg per dygn. Äggen utsöndras via urinen eller avföringen, beroende på art. Om äggen kommer i kontakt med vatten kläcks de och en annan larvform (miracidium) frigörs. Dessa söker upp speciella snäckarter, borrar sig in genom snäckans mjukdelar och utvecklas så småningom till cerkarier. En enda snäcka kan utsöndra tusentals cerkarier. | Parasiten har en invecklad livscykel med människa som värd för hon- och hanmaskar och en sötvattensnäcka som intermediär värd, i vilken det infektiösa larvstadiet utvecklas. Den i vatten fritt levande larvformen av parasiten, cerkarien, attraheras till hud, tränger igenom den och vandrar med cirkulationen till leverns blodkärl. Efter cirka en månad har larverna utvecklas till könsmogna maskar, som producerar hundratals ägg per dygn. Äggen utsöndras via urinen eller avföringen, beroende på art. Om äggen kommer i kontakt med vatten kläcks de och en annan larvform (miracidium) frigörs. Dessa söker upp speciella snäckarter, borrar sig in genom snäckans mjukdelar och utvecklas så småningom till cerkarier. En enda snäcka kan utsöndra tusentals cerkarier. | ||
| − | |||
===Symtom och klinisk bild=== | ===Symtom och klinisk bild=== | ||
| − | |||
Initialt kan överkänslighetsreaktioner, s.k. badklåda, uppträda dygnet efter parasitens penetration av huden ([[trichobilharzia spp.|fågelparasiter]] ger liknande symtom på människa). Beroende på art kan symtomen variera. Diffusa symtom under parasitens migrations- och tillväxtfas kan vara: nässelutslag, feber, magvärk, förstorad lever och mjälte (Katayamafeber). Ofta ses eosinofili. Sjukdomssymtomen orsakas framför allt av de ägg som inte utsöndras utan som blir kvar i kroppen. Ägg i vävnader orsakar inflammation och granulombildning som leder till fibros och förkalkning. Vid ''S. hematobium''-infektion skadas urinblåsan med hematuri som följd. Kronisk infektion kan leda till urinblåscancer. Vid infektion med ''S. mansoni'' och ''S. japonicum'' skadas främst levern och tarmen. I endemiska områden är infertilitet hos kvinnor ofta resultat av granulombildning runt ägg, som hamnat i äggledarna. I sällsynta fall kan man se skador i hjärnan och centrala nervsystemet orsakade av ägg, som förirrat sig till dessa vävnader. | Initialt kan överkänslighetsreaktioner, s.k. badklåda, uppträda dygnet efter parasitens penetration av huden ([[trichobilharzia spp.|fågelparasiter]] ger liknande symtom på människa). Beroende på art kan symtomen variera. Diffusa symtom under parasitens migrations- och tillväxtfas kan vara: nässelutslag, feber, magvärk, förstorad lever och mjälte (Katayamafeber). Ofta ses eosinofili. Sjukdomssymtomen orsakas framför allt av de ägg som inte utsöndras utan som blir kvar i kroppen. Ägg i vävnader orsakar inflammation och granulombildning som leder till fibros och förkalkning. Vid ''S. hematobium''-infektion skadas urinblåsan med hematuri som följd. Kronisk infektion kan leda till urinblåscancer. Vid infektion med ''S. mansoni'' och ''S. japonicum'' skadas främst levern och tarmen. I endemiska områden är infertilitet hos kvinnor ofta resultat av granulombildning runt ägg, som hamnat i äggledarna. I sällsynta fall kan man se skador i hjärnan och centrala nervsystemet orsakade av ägg, som förirrat sig till dessa vävnader. | ||
| − | |||
===Epidemiologi=== | ===Epidemiologi=== | ||
| − | |||
Sjukdomen förekommer i länder med tropiskt eller subtropiskt klimat. Åttiofem procent av de mer än 200 miljoner människor som är infekterade lever i Afrika, söder om Sahara. ''S. hematobium'' är den vanligaste arten och är endemisk i Afrika och Mellanöstern. ''S. mansoni'' förekommer i Afrika, Sydamerika (Brasilien, Surinam och Venezuela), Karibien (Puerto Rico, Santa Lucia, Guadeloupe, Martinique, Dominikanska republiken, Antigua och Monserrat) samt i vissa områden i Mellanöstern. ''S. japonicum'' finns i Kina (Changjiang-floden, Sichuan och Yunnan) och på Filippinerna. ''S. mekongi'' förekommer i områden längs med Mekongifloden i Sydostasien (Kambodja, Laos, Thailand). | Sjukdomen förekommer i länder med tropiskt eller subtropiskt klimat. Åttiofem procent av de mer än 200 miljoner människor som är infekterade lever i Afrika, söder om Sahara. ''S. hematobium'' är den vanligaste arten och är endemisk i Afrika och Mellanöstern. ''S. mansoni'' förekommer i Afrika, Sydamerika (Brasilien, Surinam och Venezuela), Karibien (Puerto Rico, Santa Lucia, Guadeloupe, Martinique, Dominikanska republiken, Antigua och Monserrat) samt i vissa områden i Mellanöstern. ''S. japonicum'' finns i Kina (Changjiang-floden, Sichuan och Yunnan) och på Filippinerna. ''S. mekongi'' förekommer i områden längs med Mekongifloden i Sydostasien (Kambodja, Laos, Thailand). | ||
| + | ==Provtagning och transport== | ||
| + | ===Urin=== | ||
| + | ====Provtagning==== | ||
| + | Urin samlas mellan klockan 10:00 och 14:00. Alternativt samlas urin under 24 timmar. Små urinvolymer på ca 10 mL accepteras, men sensitiviteten blir låg och vid negativt undersökningsresultat rekommenderas ny provtagning. | ||
| + | Se även [[Provtagning och transport|provtagningsanvisningar]] | ||
| − | + | ====Transport==== | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
Okonserverad urin bör undersökas så fort som möjligt. Undvik att sända prov i slutet av veckan eller inför en helg. Vid förväntad lång provtransport kan urinen konserveras genom tillsats av 1-2 mL 3,7 % formaldehyd (=10 % formalin) per 100 mL urin. | Okonserverad urin bör undersökas så fort som möjligt. Undvik att sända prov i slutet av veckan eller inför en helg. Vid förväntad lång provtransport kan urinen konserveras genom tillsats av 1-2 mL 3,7 % formaldehyd (=10 % formalin) per 100 mL urin. | ||
| − | ==== | + | ===Feces=== |
| − | ===== | + | ====Provtagning==== |
| + | Se [[Provtagning och transport|provtagningsanvisningar]] | ||
| + | ====Transport==== | ||
| + | Inga speciella krav. | ||
| − | + | ===Blod/serum=== | |
| − | + | ====Provtagning==== | |
| − | |||
| − | ==== | ||
Blodprov tas i rör utan tillsats. | Blodprov tas i rör utan tillsats. | ||
| − | + | ====Transport==== | |
Inga speciella krav. | Inga speciella krav. | ||
==Laboratoriediagnostik== | ==Laboratoriediagnostik== | ||
===Allmänt=== | ===Allmänt=== | ||
| + | [[Fil:S.HaemobiumÄggAM.jpg|thumb|200px|right|''S. haematobium''-ägg. ''Foto: Anders Magnusson, Smittskyddsinstitutet''.]] | ||
Eosinofili och förhöjt IgE är kännetecknande för maskinfektioner och indikerar ytterligare laboratorieundersökningar. Metoder som kan påvisa utsöndrade ägg i feces och/eller urin betraktas som referensmetoder. Vid låggradiga infektioner kan dock äggutsöndringen vara låg och intermittent och därför används även indirekta metoder (t.ex. indirekt immunfluorescens-test och ELISA) som mäter antikroppshalter i serumprover. Det finns metoder som mäter cirkulerade antigener i serum, urin, saliv och mjölk, men dessa är inte tillräckligt känsliga för att upptäcka låggradig infektion. Under senare år har ett flertal PCR-tekniker för detektion av ''Schistosoma''-DNA i feces och urin utvecklats. | Eosinofili och förhöjt IgE är kännetecknande för maskinfektioner och indikerar ytterligare laboratorieundersökningar. Metoder som kan påvisa utsöndrade ägg i feces och/eller urin betraktas som referensmetoder. Vid låggradiga infektioner kan dock äggutsöndringen vara låg och intermittent och därför används även indirekta metoder (t.ex. indirekt immunfluorescens-test och ELISA) som mäter antikroppshalter i serumprover. Det finns metoder som mäter cirkulerade antigener i serum, urin, saliv och mjölk, men dessa är inte tillräckligt känsliga för att upptäcka låggradig infektion. Under senare år har ett flertal PCR-tekniker för detektion av ''Schistosoma''-DNA i feces och urin utvecklats. | ||
| − | + | ===Referensmetod urin=== | |
| + | Mikroskopisk påvisning av maskägg (''S. hematobium,'' men även ''S. mansoni'' och i sällsynta fall ''S. japonicum'') efter filtrering och/eller centrifugering. Se bilaga [[PAR 06 Schistosoma ägg i urin|PAR 06]]. | ||
===Referensmetod feces=== | ===Referensmetod feces=== | ||
| − | + | [[Fil:S.mansoniÄggAM.jpg|thumb|200px|right|''S. mansoni''-ägg. ''Foto: Anders Magnusson, Smittskyddsinstitutet''.]] | |
| − | Mikroskopisk påvisning av maskägg efter formalin/etylacetat-koncentration av feces | + | Mikroskopisk påvisning av maskägg efter formalin/etylacetat-koncentration av feces för ''S. mansoni, S. japonicum''-, ''S. intercalatum''-och ''S. mekongi''-ägg. Se bilaga [[PAR 01 Cystor och maskägg, feces koncentration|PAR 01]]. |
| − | |||
====Avläsningskriterier==== | ====Avläsningskriterier==== | ||
| − | |||
Beskrivning av ''Schistosoma''-ägg: | Beskrivning av ''Schistosoma''-ägg: | ||
| Rad 96: | Rad 84: | ||
Kvalitetssäkring | Kvalitetssäkring | ||
Extern: INSTAND och UK NEQAS kvalitetskontroll. | Extern: INSTAND och UK NEQAS kvalitetskontroll. | ||
| − | + | ||
'''''ELISA''''' | '''''ELISA''''' | ||
Princip: enzymmärkta antikroppar mot humant immunglobulin används för att påvisa specifika antikroppar som reagerat med lösligt extrakt (antigen) av ''S. mansoni''-ägg, som bundits till en plastyta. Enzymaktiviteten mäts genom tillsats av substrat och kromogen. Avläsning sker i fotometer. | Princip: enzymmärkta antikroppar mot humant immunglobulin används för att påvisa specifika antikroppar som reagerat med lösligt extrakt (antigen) av ''S. mansoni''-ägg, som bundits till en plastyta. Enzymaktiviteten mäts genom tillsats av substrat och kromogen. Avläsning sker i fotometer. | ||
| Rad 103: | Rad 91: | ||
Extern: INSTAND och UK NEQAS kvalitetskontroll | Extern: INSTAND och UK NEQAS kvalitetskontroll | ||
| − | + | ||
'''''Western blot''''' | '''''Western blot''''' | ||
Princip: enzymmärkta antikroppar mot humant immunglobulin används för att påvisa specifika antikroppar som reagerat med antigen som separerats elektroforetiskt och bundits ett nitrocellulosa-membran. Enzymaktiviteten mäts genom tillsats av substrat och kromogen. Avläsning kan ske visuellt. | Princip: enzymmärkta antikroppar mot humant immunglobulin används för att påvisa specifika antikroppar som reagerat med antigen som separerats elektroforetiskt och bundits ett nitrocellulosa-membran. Enzymaktiviteten mäts genom tillsats av substrat och kromogen. Avläsning kan ske visuellt. | ||
=====Antigen/DNA-påvisning (se under ”Allmänt)===== | =====Antigen/DNA-påvisning (se under ”Allmänt)===== | ||
| − | + | ||
=====Kato-Katz===== | =====Kato-Katz===== | ||
| − | Kato-Katz är den klassiska referensmetoden för påvisning av ''S. mansoni''- och ''S. japonicum''-ägg i feces (7). Metoden har låg känslighet (detektiongräns 20 ägg per gram feces) och är användbar i endemiska områden. (Även maskägg från ''Ascaris'', hakmask, ''Trichuris'', ''Taenia'', och ''Enterobius'' kan detekteras med denna metod.) | + | Kato-Katz är den klassiska referensmetoden för påvisning av ''S. mansoni''- och ''S. japonicum''-ägg i feces (7). Metoden har låg känslighet (detektiongräns 20 ägg per gram feces) och är användbar i endemiska områden. (Även maskägg från ''[[Ascaris lumbricoides|Ascaris ]]'', [[Hakmask|hakmask]], ''[[Trichuris trichiura|Trichuris ]]'', ''[[Taenia saginata|Taenia ]]'', och ''[[Enterobius vermicularis|Enterobius ]]'' kan detekteras med denna metod.) |
| − | + | ||
Princip: en bestämd mängd feces pressas jämnt ut mellan ett objektsglas och en bit cellofan, som är indränkt i blandning av glycerol och malakitgrönt.Glycerol/malakitgrönt-lösningen gör provet transparent. Äggen räknas i mikroskop. Antal ägg på objektsglaset omvandlas till antal ägg per gram feces. | Princip: en bestämd mängd feces pressas jämnt ut mellan ett objektsglas och en bit cellofan, som är indränkt i blandning av glycerol och malakitgrönt.Glycerol/malakitgrönt-lösningen gör provet transparent. Äggen räknas i mikroskop. Antal ägg på objektsglaset omvandlas till antal ägg per gram feces. | ||
===Laboratorierapportering=== | ===Laboratorierapportering=== | ||
| − | Schistosomiasis är inte anmälningspliktig. | + | Schistosomiasis är inte anmälningspliktig enligt smittskyddslagen. |
==Litteraturhänvisningar== | ==Litteraturhänvisningar== | ||
| Rad 129: | Rad 117: | ||
| − | |||
[[Kategori:Parasiter]] | [[Kategori:Parasiter]] | ||
| − | |||
Nuvarande version från 17 juni 2013 kl. 14.30
Huvudartikel, publicerad augusti 2011.
Till innehållsförteckning för Referensmetodik:Parasitologisk diagnostik
Schistosoma spp.[redigera]
Smittämne[redigera]
Human schistosomiasis orsakas av parasitära blodmaskar (trematoder). Parasiten har en infektiös larvform som finns i sötvatten i endemiska områden (t.ex. Malawisjön, Viktoriasjön). De vanligaste arterna är Schistosoma mansoni, S. japonicum och S. hematobium. I mindre utsträckning förekommer arterna S. intercalatum och S. mekongi.
Livscykel[redigera]
Parasiten har en invecklad livscykel med människa som värd för hon- och hanmaskar och en sötvattensnäcka som intermediär värd, i vilken det infektiösa larvstadiet utvecklas. Den i vatten fritt levande larvformen av parasiten, cerkarien, attraheras till hud, tränger igenom den och vandrar med cirkulationen till leverns blodkärl. Efter cirka en månad har larverna utvecklas till könsmogna maskar, som producerar hundratals ägg per dygn. Äggen utsöndras via urinen eller avföringen, beroende på art. Om äggen kommer i kontakt med vatten kläcks de och en annan larvform (miracidium) frigörs. Dessa söker upp speciella snäckarter, borrar sig in genom snäckans mjukdelar och utvecklas så småningom till cerkarier. En enda snäcka kan utsöndra tusentals cerkarier.
Symtom och klinisk bild[redigera]
Initialt kan överkänslighetsreaktioner, s.k. badklåda, uppträda dygnet efter parasitens penetration av huden (fågelparasiter ger liknande symtom på människa). Beroende på art kan symtomen variera. Diffusa symtom under parasitens migrations- och tillväxtfas kan vara: nässelutslag, feber, magvärk, förstorad lever och mjälte (Katayamafeber). Ofta ses eosinofili. Sjukdomssymtomen orsakas framför allt av de ägg som inte utsöndras utan som blir kvar i kroppen. Ägg i vävnader orsakar inflammation och granulombildning som leder till fibros och förkalkning. Vid S. hematobium-infektion skadas urinblåsan med hematuri som följd. Kronisk infektion kan leda till urinblåscancer. Vid infektion med S. mansoni och S. japonicum skadas främst levern och tarmen. I endemiska områden är infertilitet hos kvinnor ofta resultat av granulombildning runt ägg, som hamnat i äggledarna. I sällsynta fall kan man se skador i hjärnan och centrala nervsystemet orsakade av ägg, som förirrat sig till dessa vävnader.
Epidemiologi[redigera]
Sjukdomen förekommer i länder med tropiskt eller subtropiskt klimat. Åttiofem procent av de mer än 200 miljoner människor som är infekterade lever i Afrika, söder om Sahara. S. hematobium är den vanligaste arten och är endemisk i Afrika och Mellanöstern. S. mansoni förekommer i Afrika, Sydamerika (Brasilien, Surinam och Venezuela), Karibien (Puerto Rico, Santa Lucia, Guadeloupe, Martinique, Dominikanska republiken, Antigua och Monserrat) samt i vissa områden i Mellanöstern. S. japonicum finns i Kina (Changjiang-floden, Sichuan och Yunnan) och på Filippinerna. S. mekongi förekommer i områden längs med Mekongifloden i Sydostasien (Kambodja, Laos, Thailand).
Provtagning och transport[redigera]
Urin[redigera]
Provtagning[redigera]
Urin samlas mellan klockan 10:00 och 14:00. Alternativt samlas urin under 24 timmar. Små urinvolymer på ca 10 mL accepteras, men sensitiviteten blir låg och vid negativt undersökningsresultat rekommenderas ny provtagning. Se även provtagningsanvisningar
Transport[redigera]
Okonserverad urin bör undersökas så fort som möjligt. Undvik att sända prov i slutet av veckan eller inför en helg. Vid förväntad lång provtransport kan urinen konserveras genom tillsats av 1-2 mL 3,7 % formaldehyd (=10 % formalin) per 100 mL urin.
Feces[redigera]
Provtagning[redigera]
Transport[redigera]
Inga speciella krav.
Blod/serum[redigera]
Provtagning[redigera]
Blodprov tas i rör utan tillsats.
Transport[redigera]
Inga speciella krav.
Laboratoriediagnostik[redigera]
Allmänt[redigera]
Eosinofili och förhöjt IgE är kännetecknande för maskinfektioner och indikerar ytterligare laboratorieundersökningar. Metoder som kan påvisa utsöndrade ägg i feces och/eller urin betraktas som referensmetoder. Vid låggradiga infektioner kan dock äggutsöndringen vara låg och intermittent och därför används även indirekta metoder (t.ex. indirekt immunfluorescens-test och ELISA) som mäter antikroppshalter i serumprover. Det finns metoder som mäter cirkulerade antigener i serum, urin, saliv och mjölk, men dessa är inte tillräckligt känsliga för att upptäcka låggradig infektion. Under senare år har ett flertal PCR-tekniker för detektion av Schistosoma-DNA i feces och urin utvecklats.
Referensmetod urin[redigera]
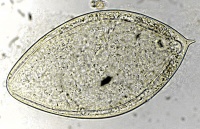
Mikroskopisk påvisning av maskägg (S. hematobium, men även S. mansoni och i sällsynta fall S. japonicum) efter filtrering och/eller centrifugering. Se bilaga PAR 06.
Referensmetod feces[redigera]
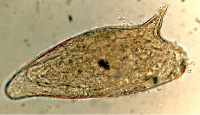
Mikroskopisk påvisning av maskägg efter formalin/etylacetat-koncentration av feces för S. mansoni, S. japonicum-, S. intercalatum-och S. mekongi-ägg. Se bilaga PAR 01.
Avläsningskriterier[redigera]
Beskrivning av Schistosoma-ägg:
| Art | Form | Storlek (mikrometer) | Karaktäristika |
|---|---|---|---|
| S. mansoni | ovalt | 114-175 x 45-70 | sidoställd tagg |
| S. hematobium | ovalt | 112-170 x 50-70 | terminal tagg |
| S. japonicum | runt | 70-100 x 55-65 | sidoställd knopp |
| S. intercalatum | avlångt | 140-240 x 50-70 | terminal tagg |
| S. mekongi | runt | 51-73 x 39-66 | knappt synlig knopp |
Alla arter har ett genomskinligt äggskal och innehåller ett miracidium. Tomma ägg och fria miracidier kan förekomma.
Kvalitetssäkring feces[redigera]
Externkontroll: Schistosoma-ägg ingår i UK-NEQAS utskick
Svarsrutiner feces[redigera]
Negativt prov utsvaras: ”Cystor/maskägg koncentrationsprov: Inga Schistosoma spp.-ägg påvisade.”
Positivt prov utsvaras: ”Cystor/maskägg koncentrationsprov: Ägg av Schistosoma (ange species) påvisade.”
Övriga metoder[redigera]
Äggpåvisning i biopsiprov från tarmen efter prokto- eller rektoskopi.[redigera]
Provet kan direkt undersökas i mikroskop efter förekomst av levande eller döda ägg.
Antikroppspåvisning[redigera]
Indirekt immunfluorescensmetod Princip (8): fluorescerande antikroppar mot humant immunglobulin används för att påvisa specifika antikroppar som reagerat med fryssnitt av S. mansoni-maskar. Kvalitetssäkring Extern: INSTAND och UK NEQAS kvalitetskontroll.
ELISA Princip: enzymmärkta antikroppar mot humant immunglobulin används för att påvisa specifika antikroppar som reagerat med lösligt extrakt (antigen) av S. mansoni-ägg, som bundits till en plastyta. Enzymaktiviteten mäts genom tillsats av substrat och kromogen. Avläsning sker i fotometer.
Kvalitetssäkring
Extern: INSTAND och UK NEQAS kvalitetskontroll
Western blot Princip: enzymmärkta antikroppar mot humant immunglobulin används för att påvisa specifika antikroppar som reagerat med antigen som separerats elektroforetiskt och bundits ett nitrocellulosa-membran. Enzymaktiviteten mäts genom tillsats av substrat och kromogen. Avläsning kan ske visuellt.
Antigen/DNA-påvisning (se under ”Allmänt)[redigera]
Kato-Katz[redigera]
Kato-Katz är den klassiska referensmetoden för påvisning av S. mansoni- och S. japonicum-ägg i feces (7). Metoden har låg känslighet (detektiongräns 20 ägg per gram feces) och är användbar i endemiska områden. (Även maskägg från Ascaris , hakmask, Trichuris , Taenia , och Enterobius kan detekteras med denna metod.)
Princip: en bestämd mängd feces pressas jämnt ut mellan ett objektsglas och en bit cellofan, som är indränkt i blandning av glycerol och malakitgrönt.Glycerol/malakitgrönt-lösningen gör provet transparent. Äggen räknas i mikroskop. Antal ägg på objektsglaset omvandlas till antal ägg per gram feces.
Laboratorierapportering[redigera]
Schistosomiasis är inte anmälningspliktig enligt smittskyddslagen.
Litteraturhänvisningar[redigera]
1. Utzinger J, N'goran EK, Caffrey CR, Keiser J. From innovation to application: social-ecological context, diagnostics, drugs and integrated control of schistosomiasis. Acta Trop. 2011 Sep;120 Suppl 1:S121-37.
2. Gomes LI, Dos Santos Marques LH, Enk MJ, de Oliveira MC, Coelho PM, Rabello A. Development and evaluation of a sensitive PCR-ELISA system for detection of schistosoma infection in feces. PLoS Negl Trop Dis. 2010 Apr 20;4(4):e664.
3. Katz N, Chaves A, Pellegrino J. A simple device for quantitative stool thick-smear technique in Schistosomiasis mansoni. Rev Inst Med Trop Sao Paulo 1972, 14: 397-400.
4. Nash TE. 1978. Antibody response to a polysaccaride antigen present in the schistosome gut. I. Sensitivity and specificity. American Journal of Tropical Medicine & Hygiene 1978, 27: 939-43.