Skillnad mellan versioner av "Influensa A, B"
| (50 mellanliggande sidversioner av 2 användare visas inte) | |||
| Rad 1: | Rad 1: | ||
| + | '''Huvudartikel''' | ||
| + | |||
| + | '''Artiklen är uppdaterad januari 2010''' | ||
| + | ---- | ||
| + | Till förgreningssidan ''[[Influensa]]'' för fler artiklar om influensa/influensavirus | ||
| + | ---- | ||
| + | |||
Till innehållsförteckningen för ''[[Referensmetodik: Nedre luftvägsinfektioner, 2:a upplagan 2005]]'' | Till innehållsförteckningen för ''[[Referensmetodik: Nedre luftvägsinfektioner, 2:a upplagan 2005]]'' | ||
---- | ---- | ||
| + | [[Fil:luft-figur11.jpg|thumb|left|450px|]] | ||
| + | |||
| + | == Influensa A, B == | ||
| + | |||
| + | === Smittämnen === | ||
| + | |||
| + | Influensavirus tillhör gruppen ortomyxovirus. De är höljeförsedda virus som infekterar luftvägarna. | ||
| + | |||
| + | Den genetiska informationen består av enkelstängad ribonukleinsyra (RNA) med negativ polaritet. Det finns 3 typer av influensavirus, A, B och [[Influensa C virus|C]] ('''tabell 15'''). Andfåglar är influensavirus A ursprungliga värdar. Hos dem infekteras tarmen, men de blir nästan aldrig sjuka av influensa. De bär på många olika subtyper av influensa A, men bara ett fåtal har givit epidemier hos människa. Två H-subtyper, H5 och H7, kan bli högpatogena om de smittar från andfågel till hönsfåglar. Fall av svår lunginflammation orsakade av influensa A/H5 har under 1997 och sedan 2003 rapporterats från Sydostasien, Afrika, Europa och Mellanöstern. | ||
| + | |||
| + | Influensa innehåller 8 separata gensegment som kodar för 10-11 proteiner. Ett par av de interna proteinerna är unika för respektive typ av influensa. Influensavirus bär på sin yta två utskott, hemagglutinin (H) och neuraminidas (N). Det finns 16 olika H och 9 olika N i influensavirus från fåglar. Kombinationen av H och N bestämmer subtypen av influensa A ('''tabell 15'''). H binder virus till receptorn (sialinsyra) på cellytan. Om vi har antikroppar mot ett visst H är vi skyddade mot alla virus som bär just detta H. | ||
| + | * '''Tabell 15.''' Olika influensatyper och viktiga karakteristika för dessa | ||
| + | {| class="wikitable" border="1" | ||
| + | |- | ||
| + | ! Influensatyp | ||
| + | ! Värd | ||
| + | ! Subtyper hos fåglar | ||
| + | ! Subtyper hos människa | ||
| + | ! Sjukdom | ||
| + | |- | ||
| + | | A | ||
| + | | Fåglar, däggdjur | ||
| + | | H1N1-H16N9; >80 kombinationer identifierade | ||
| + | | H1N1, H1N2, H2N2, H3N2, H5N1*, H7N2, H9N1* | ||
| + | | Typisk influensa | ||
| + | |- | ||
| + | | B | ||
| + | | Människa | ||
| + | | - | ||
| + | | Finns ej | ||
| + | | Typisk influensa | ||
| + | |- | ||
| + | | C | ||
| + | | Människa | ||
| + | | - | ||
| + | | Finns ej | ||
| + | | Förkylning | ||
| + | |} | ||
| + | -*Har ej orsakat epidemier; mänskliga fall har identifierats under det senaste decenniet. | ||
| − | |||
| + | Alla influensastammar som karakteriserats inom ramen för WHO:s influensaövervakning namnges. Principen för hur detta sker framgår av '''tabell 16'''. Det virus som beskrivs är alltså det 10:e influensa A-viruset som isolerats från människa i Brisbane 2007. De virus som har stor likhet med detta virus beskrivs som ”A/Brisbane/10/07-lika”. Subtyper av influensavirus som orsakat pandemier eller pandemihot finns översiktligt redovisade i '''Fig 12'''. | ||
| − | |||
| − | + | *'''Tabell 16.''' Internationella principer för hur en influensastam namnges | |
| − | + | {| class="wikitable" border="1" | |
| + | |- | ||
| + | ! Princip | ||
| + | ! Exempel | ||
| + | |- | ||
| + | | ''Virus och typ'' | ||
| + | | Influensa A | ||
| + | |- | ||
| + | | ''Från djurslag'' (anges ej för stammar från människa) | ||
| + | | (''ch''; chicken ''sw''; swine ''eq''; equine) | ||
| + | |- | ||
| + | | ''Stad eller plats'' där virus isolerats | ||
| + | | Influensa A/''Brisbane'' | ||
| + | |- | ||
| + | | ''Isoleringsnummer'' under ''aktuellt år'' | ||
| + | | Influensa A/''Brisbane/10/07'' | ||
| + | |- | ||
| + | | Subtyp | ||
| + | | Influensa A/''Brisbane/10/07(H3N2)'' | ||
| + | |} | ||
| + | ---- | ||
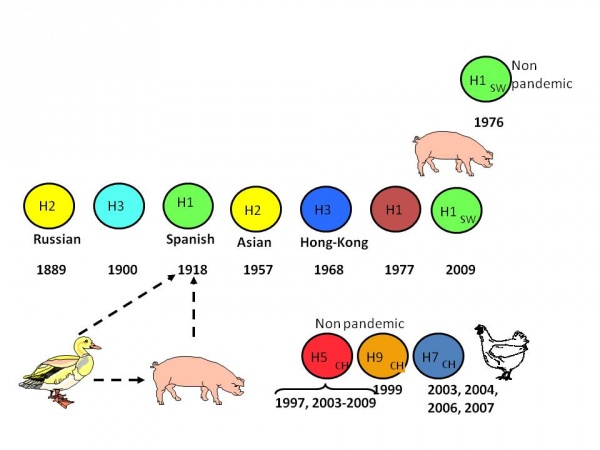
| + | [[Fil:Pandemi.jpg|thumb|center|600px| '''Fig 12'''. Subtyper av influensa som orsakat pandemi- eller pandemihot sedan 1889.]] | ||
| − | + | === Patogenes och patofysiologi === | |
| + | |||
| + | Trots att influensavirus hittas nästan uteslutande i luftvägarna är allmänsymtomen dominerande. Immunologiska signalsubstanser som induceras av infektionen och sprids i hela kroppen är sannolikt orsaken. Mängden signalsubstanser som bildas är relaterad till den mängd influensavirus som produceras. Ju mera virus som bildas desto sjukare blir man. | ||
| + | === Symtom och klinisk bild === | ||
| − | + | Influensa A och B ger karakteristisk influensasjukdom ('''tabell 17'''). Det vanligaste symtomet är torrhosta. Det som mest skiljer influensa från andra virala luftvägsinfektioner är det plötsliga insjuknandet, muskelvärken och den påtagliga allmänpåverkan. Hos personer med partiell immunitet kan man få alla grader av sjukdom, och en övergående influensareplikation i luftvägarna kan vara totalt symtomlös eller ge endast lätt snuva. | |
| − | |||
| − | Influensa A | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| + | |||
| + | *'''Tabell 17.''' Typiska influensasymtom, smittvägar och inkubationstid | ||
| + | {| class="wikitable" border="1" | ||
| + | |- | ||
| + | ! Typiska influensasymtom | ||
| + | ! Smittväg, smittsamhet | ||
| + | ! Inkubationstid | ||
| + | |- | ||
| + | | Plötsligt insättande, hög feber föregången av frysningar. | ||
| + | Muskelvärk. | ||
| + | Ordentlig sjukdomskänsla. | ||
| − | + | Torrhosta på grund av trakeit. | |
| − | |||
| − | + | (Halsont och gastroenteritsymtom vanliga hos barn) | |
| − | + | | Luftburen, aerosol. | |
| − | + | Patienten är smittsam så länge han/hon har feber. | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | Ju svårare sjukdom, desto mera virus och desto större smittsamhet. | |
| − | + | | 2-5 dagar | |
| − | + | |} | |
| − | |||
| − | + | === Epidemiologi === | |
| − | + | ||
| − | + | Influensavirus sprids mycket effektivt. Det smittar dels genom aerosol, och kan sväva länge i luften på mycket små (10µ) partiklar, dels via kontaminerade fingrar. En tumregel är att ju sjukare man är, desto mera virus utsöndras och desto mer smittar man. Influensa sprids under respektive vintersäsong på norra och södra halvklotet. Vid ekvatorn cirkulerar influensan kontinuerligt men har något högre aktivitet vid höst och vår. Anledningen till årstidsvariationerna är oklar, men att många personer vistas länge i samma rum på skolor och arbetsplatser bidrar till spridningen. Man har även visat att lufttemperaturen och luftfuktigheten påverkar aerosolsmitta. Vid låg temperatur är det lägre luftfuktighet viklet gör att luftburen smitta underlättas. Aerosolerna som bildas vid hostningar blir stabilare och mindre vilket gör att de kan sväva längre sträcka och tid vid låg luftfuktighet. Detta gynnar aerosolsmitta. Vid pandemi kan dock influensan spridas utför de vanliga säsongerna. Vid pandemin 2009 kom den första influensavågen i Storbritannien redan under sommaren. Denna spridning utanför den vanliga säsongen sker när många i populationen är naiva för den nya influensaviruset. | |
| − | + | ||
| − | + | Vi kan sjukna i influensa betydligt oftare än man skulle kunna tro med tanke på det begränsade antalet typer och subtyper. Detta beror på att influensavirus kan förändra sin yta och bli oigenkännligt för immunsystemet på många sätt ('''Tabell 18'''). | |
| − | |||
| − | |||
| − | |||
| − | |||
| + | === Prevention === | ||
| − | |||
| − | |||
| − | |||
| − | |||
Om skydd mot influensa behövs är vaccin förstahandsprofylax, men vid institutionsutbrott som berör personer med risk för svår influensasjukdom kan profylaktisk behandling övervägas. Andra överväganden kan komma att behövas om effektivt vaccin saknas. | Om skydd mot influensa behövs är vaccin förstahandsprofylax, men vid institutionsutbrott som berör personer med risk för svår influensasjukdom kan profylaktisk behandling övervägas. Andra överväganden kan komma att behövas om effektivt vaccin saknas. | ||
| − | |||
| − | Tabell 18. Hur influensavirus förändras för att undgå immunsystemet | + | Influensavaccin framställs genom att de influensastammar som väntas för året renas oftast fram från chorio-allantoisvätskan i infekterade hönsägg. Vid WHO beslutas i februari vilka stammar som ska ingå det vaccin som ska användas på hösten på norra halvklotet och i september för det som ska användas under hösten på södra halvklotet. |
| − | Typ av förändring Mekanism Virustyp som drabbas Exempel | + | |
| − | Överföring av intakt djurvirus Intakt fågelvirus eller grisvirus smittar människa. | + | Vaccinets skyddseffekt varar ca 9 månader. Den som bör/vill ha skydd mot influensa måste alltså vaccineras årligen, oavsett om en ny stam dykt upp eller inte. Neuramidashämmare är antivirala substanser som förhindrar virus spridning från cell till cell. Två neuraminidashämmare finns registrerade, Zanamivir (Relenza®) och Oseltamivir (Tamiflu®). Det svenska Läkemedelsverket och Referensgruppen för Antiviral terapi (RAV) rekommenderar att man överväger behandling med neuraminidashämmare vid svår influensasjukdom och för de medicinska riskgrupperna, förutsatt att influensaförekomst verifierats i samhället eller hos patienten. Både Tamiflu och Relenza är registrerade för profylax. Skyddseffekten är ca 90 % vid medicinering under 7 dagar, när preparatet insatts inom 48 timmar efter exposition eller vid långtidsbehandling under 6 veckor mot samhällsförvärvad influensa. |
| − | Aviär influensa Hong Kong 1997, Sydostasien 2003- | + | |
| − | Antigent skifte En gris infekteras av fågelvirus och humanvirus samtidigt, och ny subtyp uppkommer genom | + | |
| − | + | *'''Tabell 18.''' Hur influensavirus förändras för att undgå immunsystemet | |
| − | Antigen drift Mutationer i HA-genen | + | {| class="wikitable" border="1" |
| + | |- | ||
| + | ! Typ av förändring | ||
| + | ! Mekanism | ||
| + | ! Virustyp som drabbas | ||
| + | ! Exempel | ||
| + | |- | ||
| + | | Överföring av intakt djurvirus | ||
| + | | Intakt fågelvirus eller grisvirus smittar människa. | ||
| + | | Influensa A | ||
| + | | Spanska sjukan 1918, pandemi Aviär influensa Hong Kong 1997, Sydostasien 2003- och nya influensan från gris 2009 | ||
| + | |- | ||
| + | | Antigent skifte | ||
| + | | En gris infekteras av fågelvirus och humanvirus samtidigt, och ny subtyp uppkommer genom genblandning | ||
| + | | Influensa A | ||
| + | | "Asiaten" 1957, Hong Kong 1968 | ||
| + | |- | ||
| + | | Antigen drift | ||
| + | | Mutationer i HA-genen | ||
| + | | Influensa A, B | ||
| + | | De H1, H3, och B-stammar som fått bytas ut i influensavaccinet sedan respektive subtyp kom | ||
| + | |} | ||
| + | |||
| + | ==Provtagning== | ||
| + | Se [[Nedre luftvägsinfektioner orsakade av virus-provtagning]] | ||
| + | |||
| + | == Laboratoriediagnostik == | ||
| + | [[Influensa A, B-laboratoriediagnostik|Följ länken för detaljerad beskrivning]] | ||
| + | |||
| + | De viktigaste metoderna för influensadiagnostik är agenspåvisning genom antigendetektion, odling eller PCR. IgM-svaret vid influensainfektion är varierande, och analys av specifikt IgM har låg diagnostisk signifikans. Odling är referensmetodik. | ||
| + | |||
| + | == Misstänkt aviär influensa eller ny influensastam. == | ||
| + | |||
| + | Om en patient misstänks vara smittad med en influensastam som inte tidigare förekommit i samhället bör prov skickas direkt till Folkhälsomyndigheten för analys. Vid Folkhälsomyndigheten görs virusisolering i BSL-3 eller BSL-4 ([[Särskild laboratoriekapacitet på Folkhälsomyndigheten|P3+ eller P4]]) beroende på patogenicitetsgrad hos misstänkt virus. RNA extraheras, och PCR mot kända, humaninfekterande influensa typer- och subtyper görs. Subtypningsspecifika PCR-system för H1, H2, H3, H5 och H7 finns i dag etablerade på Folkhälsomyndigheten. Om test med generella primers för matrix är positivt, men PCR för H negativt görs subtypning genom direktsekvensering eller genom sekvensering av odlat material. Vid förändringar i influensaepidemiologin, som kan innebära pandemihot sker regelbunden uppdatering av instruktioner avseende provtagning etc. på Folkhälsomyndighetens hemsida. | ||
| + | |||
| + | Vid pandemins utbrott 2009 med nya influensan A (H1N1) ställdes den första diagnosen via PCR-matrixpositivt prov som var negativt för säsongs H1 och H3 PCR. Prover isolerades i BSL-3 för att sedan sekvenseras. När det fanns ett positivt isolat kunde specifk PCR utvecklas och etableras. | ||
| + | |||
| + | == Svarsrutin inklusive referensförfarande == | ||
| + | |||
| + | När influensavirus isolerats, verifierats och om indicerat, typats, svaras: Influensa, typ, eventuell subtyp påvisat vid odling i vävnadskultur, och typning med (använd metod). | ||
| + | |||
| + | Om vidare undersökning är indicerad skickas material vidare till WHO’s referenslaboratorium i Mill Hill i England. | ||
| + | |||
| + | == Laboratorierapportering == | ||
| + | Anmäles enligt [[Fågelinfluensa H5N1|gällande falldefinition-fågelinfluensa]] och [[Influensa A(H1N1)pdm09|gällande falldefinition-influensa A (H1N1)]] | ||
| + | |||
| + | Influensa är för övrigt inte en anmälningspliktig sjukdom. I samband med pandemin 2009 (Influensa A(H1N1)pdm09) var den dock anmälningsplikig. Detta för att man möjliggöra smittspårning vid alla fall för att förhindra smittspridning i samhället och senare för att följa pandemins förlopp. | ||
| + | |||
| + | Hösten 1993 initierades ett system där alla laboratorier som bedriver influensadiagnostik veckovis till SMI (numera Folkhälsomyndigheten) rapporterar antal influensadiagnoser, samt patienternas kön och ålder. Systemet har fungerat mycket bra, och under epidemiår har mer än 2 diagnoser/10<math>^5</math> invånare rapporterats, vilket internationellt sett sannolikt är mycket. Under 2006 startades ett sentinelprovtagningssytem för att kunna övervaka säsongsinfluensans spridning i samhället. En del av de prover som inkommer via sentinelprovtagningen karaktäriseras. Laboratorierapporterna och rapporter om klinisk influensa från utvalda läkare över hela Sverige sammanställs varje vecka på Folkhälsomyndighetens hemsida. | ||
| + | |||
| + | I samband med pandemin 2009 startades flera olika rapporteringssytem. Alla laboratorieverifierade fall anmäldes i SMILab, alla laboratorier rapporterade antal utförda analyser samt antalet positiva diagnoser. Flera olika epidemiologiska system utvärderades som övervakningssytem. Under pandemin sammanställdes veckorapporter med uppgifter från alla övervakningssystem. | ||
| + | |||
| + | ==Referensfunktioner== | ||
| + | Enligt [[virologisk R-lista]] | ||
| + | == REFERENSER == | ||
| + | *Diagnostic Procedures for Viral, Rikettsial, and Chlamydial Infections. 7th Edition. Edwin H. Lennette PhD, David A. Lennette PhD, Evelyne T. Lennette PhD. | ||
| − | + | *Textbook of influenza; Blackwell science, ltd, Oxford 1998, Nicholson K, Webster J and Hay A. | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | [[Kategori:Nedre luftvägsinfektioner]] | |
| − | |||
| − | |||
Nuvarande version från 14 januari 2014 kl. 13.54
Huvudartikel
Artiklen är uppdaterad januari 2010
Till förgreningssidan Influensa för fler artiklar om influensa/influensavirus
Till innehållsförteckningen för Referensmetodik: Nedre luftvägsinfektioner, 2:a upplagan 2005
Influensa A, B[redigera]
Smittämnen[redigera]
Influensavirus tillhör gruppen ortomyxovirus. De är höljeförsedda virus som infekterar luftvägarna.
Den genetiska informationen består av enkelstängad ribonukleinsyra (RNA) med negativ polaritet. Det finns 3 typer av influensavirus, A, B och C (tabell 15). Andfåglar är influensavirus A ursprungliga värdar. Hos dem infekteras tarmen, men de blir nästan aldrig sjuka av influensa. De bär på många olika subtyper av influensa A, men bara ett fåtal har givit epidemier hos människa. Två H-subtyper, H5 och H7, kan bli högpatogena om de smittar från andfågel till hönsfåglar. Fall av svår lunginflammation orsakade av influensa A/H5 har under 1997 och sedan 2003 rapporterats från Sydostasien, Afrika, Europa och Mellanöstern.
Influensa innehåller 8 separata gensegment som kodar för 10-11 proteiner. Ett par av de interna proteinerna är unika för respektive typ av influensa. Influensavirus bär på sin yta två utskott, hemagglutinin (H) och neuraminidas (N). Det finns 16 olika H och 9 olika N i influensavirus från fåglar. Kombinationen av H och N bestämmer subtypen av influensa A (tabell 15). H binder virus till receptorn (sialinsyra) på cellytan. Om vi har antikroppar mot ett visst H är vi skyddade mot alla virus som bär just detta H.
- Tabell 15. Olika influensatyper och viktiga karakteristika för dessa
| Influensatyp | Värd | Subtyper hos fåglar | Subtyper hos människa | Sjukdom |
|---|---|---|---|---|
| A | Fåglar, däggdjur | H1N1-H16N9; >80 kombinationer identifierade | H1N1, H1N2, H2N2, H3N2, H5N1*, H7N2, H9N1* | Typisk influensa |
| B | Människa | - | Finns ej | Typisk influensa |
| C | Människa | - | Finns ej | Förkylning |
-*Har ej orsakat epidemier; mänskliga fall har identifierats under det senaste decenniet.
Alla influensastammar som karakteriserats inom ramen för WHO:s influensaövervakning namnges. Principen för hur detta sker framgår av tabell 16. Det virus som beskrivs är alltså det 10:e influensa A-viruset som isolerats från människa i Brisbane 2007. De virus som har stor likhet med detta virus beskrivs som ”A/Brisbane/10/07-lika”. Subtyper av influensavirus som orsakat pandemier eller pandemihot finns översiktligt redovisade i Fig 12.
- Tabell 16. Internationella principer för hur en influensastam namnges
| Princip | Exempel |
|---|---|
| Virus och typ | Influensa A |
| Från djurslag (anges ej för stammar från människa) | (ch; chicken sw; swine eq; equine) |
| Stad eller plats där virus isolerats | Influensa A/Brisbane |
| Isoleringsnummer under aktuellt år | Influensa A/Brisbane/10/07 |
| Subtyp | Influensa A/Brisbane/10/07(H3N2) |
Patogenes och patofysiologi[redigera]
Trots att influensavirus hittas nästan uteslutande i luftvägarna är allmänsymtomen dominerande. Immunologiska signalsubstanser som induceras av infektionen och sprids i hela kroppen är sannolikt orsaken. Mängden signalsubstanser som bildas är relaterad till den mängd influensavirus som produceras. Ju mera virus som bildas desto sjukare blir man.
Symtom och klinisk bild[redigera]
Influensa A och B ger karakteristisk influensasjukdom (tabell 17). Det vanligaste symtomet är torrhosta. Det som mest skiljer influensa från andra virala luftvägsinfektioner är det plötsliga insjuknandet, muskelvärken och den påtagliga allmänpåverkan. Hos personer med partiell immunitet kan man få alla grader av sjukdom, och en övergående influensareplikation i luftvägarna kan vara totalt symtomlös eller ge endast lätt snuva.
- Tabell 17. Typiska influensasymtom, smittvägar och inkubationstid
| Typiska influensasymtom | Smittväg, smittsamhet | Inkubationstid |
|---|---|---|
| Plötsligt insättande, hög feber föregången av frysningar.
Muskelvärk. Ordentlig sjukdomskänsla. Torrhosta på grund av trakeit. (Halsont och gastroenteritsymtom vanliga hos barn) |
Luftburen, aerosol.
Patienten är smittsam så länge han/hon har feber. Ju svårare sjukdom, desto mera virus och desto större smittsamhet. |
2-5 dagar |
Epidemiologi[redigera]
Influensavirus sprids mycket effektivt. Det smittar dels genom aerosol, och kan sväva länge i luften på mycket små (10µ) partiklar, dels via kontaminerade fingrar. En tumregel är att ju sjukare man är, desto mera virus utsöndras och desto mer smittar man. Influensa sprids under respektive vintersäsong på norra och södra halvklotet. Vid ekvatorn cirkulerar influensan kontinuerligt men har något högre aktivitet vid höst och vår. Anledningen till årstidsvariationerna är oklar, men att många personer vistas länge i samma rum på skolor och arbetsplatser bidrar till spridningen. Man har även visat att lufttemperaturen och luftfuktigheten påverkar aerosolsmitta. Vid låg temperatur är det lägre luftfuktighet viklet gör att luftburen smitta underlättas. Aerosolerna som bildas vid hostningar blir stabilare och mindre vilket gör att de kan sväva längre sträcka och tid vid låg luftfuktighet. Detta gynnar aerosolsmitta. Vid pandemi kan dock influensan spridas utför de vanliga säsongerna. Vid pandemin 2009 kom den första influensavågen i Storbritannien redan under sommaren. Denna spridning utanför den vanliga säsongen sker när många i populationen är naiva för den nya influensaviruset.
Vi kan sjukna i influensa betydligt oftare än man skulle kunna tro med tanke på det begränsade antalet typer och subtyper. Detta beror på att influensavirus kan förändra sin yta och bli oigenkännligt för immunsystemet på många sätt (Tabell 18).
Prevention[redigera]
Om skydd mot influensa behövs är vaccin förstahandsprofylax, men vid institutionsutbrott som berör personer med risk för svår influensasjukdom kan profylaktisk behandling övervägas. Andra överväganden kan komma att behövas om effektivt vaccin saknas.
Influensavaccin framställs genom att de influensastammar som väntas för året renas oftast fram från chorio-allantoisvätskan i infekterade hönsägg. Vid WHO beslutas i februari vilka stammar som ska ingå det vaccin som ska användas på hösten på norra halvklotet och i september för det som ska användas under hösten på södra halvklotet.
Vaccinets skyddseffekt varar ca 9 månader. Den som bör/vill ha skydd mot influensa måste alltså vaccineras årligen, oavsett om en ny stam dykt upp eller inte. Neuramidashämmare är antivirala substanser som förhindrar virus spridning från cell till cell. Två neuraminidashämmare finns registrerade, Zanamivir (Relenza®) och Oseltamivir (Tamiflu®). Det svenska Läkemedelsverket och Referensgruppen för Antiviral terapi (RAV) rekommenderar att man överväger behandling med neuraminidashämmare vid svår influensasjukdom och för de medicinska riskgrupperna, förutsatt att influensaförekomst verifierats i samhället eller hos patienten. Både Tamiflu och Relenza är registrerade för profylax. Skyddseffekten är ca 90 % vid medicinering under 7 dagar, när preparatet insatts inom 48 timmar efter exposition eller vid långtidsbehandling under 6 veckor mot samhällsförvärvad influensa.
- Tabell 18. Hur influensavirus förändras för att undgå immunsystemet
| Typ av förändring | Mekanism | Virustyp som drabbas | Exempel |
|---|---|---|---|
| Överföring av intakt djurvirus | Intakt fågelvirus eller grisvirus smittar människa. | Influensa A | Spanska sjukan 1918, pandemi Aviär influensa Hong Kong 1997, Sydostasien 2003- och nya influensan från gris 2009 |
| Antigent skifte | En gris infekteras av fågelvirus och humanvirus samtidigt, och ny subtyp uppkommer genom genblandning | Influensa A | "Asiaten" 1957, Hong Kong 1968 |
| Antigen drift | Mutationer i HA-genen | Influensa A, B | De H1, H3, och B-stammar som fått bytas ut i influensavaccinet sedan respektive subtyp kom |
Provtagning[redigera]
Se Nedre luftvägsinfektioner orsakade av virus-provtagning
Laboratoriediagnostik[redigera]
Följ länken för detaljerad beskrivning
De viktigaste metoderna för influensadiagnostik är agenspåvisning genom antigendetektion, odling eller PCR. IgM-svaret vid influensainfektion är varierande, och analys av specifikt IgM har låg diagnostisk signifikans. Odling är referensmetodik.
Misstänkt aviär influensa eller ny influensastam.[redigera]
Om en patient misstänks vara smittad med en influensastam som inte tidigare förekommit i samhället bör prov skickas direkt till Folkhälsomyndigheten för analys. Vid Folkhälsomyndigheten görs virusisolering i BSL-3 eller BSL-4 (P3+ eller P4) beroende på patogenicitetsgrad hos misstänkt virus. RNA extraheras, och PCR mot kända, humaninfekterande influensa typer- och subtyper görs. Subtypningsspecifika PCR-system för H1, H2, H3, H5 och H7 finns i dag etablerade på Folkhälsomyndigheten. Om test med generella primers för matrix är positivt, men PCR för H negativt görs subtypning genom direktsekvensering eller genom sekvensering av odlat material. Vid förändringar i influensaepidemiologin, som kan innebära pandemihot sker regelbunden uppdatering av instruktioner avseende provtagning etc. på Folkhälsomyndighetens hemsida.
Vid pandemins utbrott 2009 med nya influensan A (H1N1) ställdes den första diagnosen via PCR-matrixpositivt prov som var negativt för säsongs H1 och H3 PCR. Prover isolerades i BSL-3 för att sedan sekvenseras. När det fanns ett positivt isolat kunde specifk PCR utvecklas och etableras.
Svarsrutin inklusive referensförfarande[redigera]
När influensavirus isolerats, verifierats och om indicerat, typats, svaras: Influensa, typ, eventuell subtyp påvisat vid odling i vävnadskultur, och typning med (använd metod).
Om vidare undersökning är indicerad skickas material vidare till WHO’s referenslaboratorium i Mill Hill i England.
Laboratorierapportering[redigera]
Anmäles enligt gällande falldefinition-fågelinfluensa och gällande falldefinition-influensa A (H1N1)
Influensa är för övrigt inte en anmälningspliktig sjukdom. I samband med pandemin 2009 (Influensa A(H1N1)pdm09) var den dock anmälningsplikig. Detta för att man möjliggöra smittspårning vid alla fall för att förhindra smittspridning i samhället och senare för att följa pandemins förlopp.
Hösten 1993 initierades ett system där alla laboratorier som bedriver influensadiagnostik veckovis till SMI (numera Folkhälsomyndigheten) rapporterar antal influensadiagnoser, samt patienternas kön och ålder. Systemet har fungerat mycket bra, och under epidemiår har mer än 2 diagnoser/10Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://wikimedia.org/api/rest_v1/":): {\displaystyle ^5} invånare rapporterats, vilket internationellt sett sannolikt är mycket. Under 2006 startades ett sentinelprovtagningssytem för att kunna övervaka säsongsinfluensans spridning i samhället. En del av de prover som inkommer via sentinelprovtagningen karaktäriseras. Laboratorierapporterna och rapporter om klinisk influensa från utvalda läkare över hela Sverige sammanställs varje vecka på Folkhälsomyndighetens hemsida.
I samband med pandemin 2009 startades flera olika rapporteringssytem. Alla laboratorieverifierade fall anmäldes i SMILab, alla laboratorier rapporterade antal utförda analyser samt antalet positiva diagnoser. Flera olika epidemiologiska system utvärderades som övervakningssytem. Under pandemin sammanställdes veckorapporter med uppgifter från alla övervakningssystem.
Referensfunktioner[redigera]
Enligt virologisk R-lista
REFERENSER[redigera]
- Diagnostic Procedures for Viral, Rikettsial, and Chlamydial Infections. 7th Edition. Edwin H. Lennette PhD, David A. Lennette PhD, Evelyne T. Lennette PhD.
- Textbook of influenza; Blackwell science, ltd, Oxford 1998, Nicholson K, Webster J and Hay A.