Skillnad mellan versioner av "Speciell epidemiologi-infektioner i mage och tarm"
| Rad 31: | Rad 31: | ||
'''Tyfoid- och paratyfoidfeber''' | '''Tyfoid- och paratyfoidfeber''' | ||
| − | ''S.'' Typhi och ''S.'' Paratyphi har endast människa som reservoar. De rapporterade fallen av tyfoidfeber har varit ganska konstant under | + | ''S.'' Typhi och ''S.'' Paratyphi har endast människa som reservoar. De rapporterade fallen av tyfoidfeber har varit ganska konstant under många år. Under 1999 noterades ett utbrott av paratyfoidfeber i den turkiska turistorten Alanya då 305 europeiska turister smittades varav 80 svenskar. De inhemska fall som inträffat har varit sekundärfall eller laboratoriesmitta. Den senaste tio-årsperioden (2002-2011) rapporterades cirka 10 - 30 fall/år, praktisk taget alla smittade utomlands. Ett undantag var ett mindre utbrott med paratyfoid i Skåne 2007 som drabbade 16 personer. |
Två olika vacciner mot tyfoid finns. Ett levande attenuerat och ett innehållande Vi-antigen. | Två olika vacciner mot tyfoid finns. Ett levande attenuerat och ett innehållande Vi-antigen. | ||
Versionen från 22 april 2012 kl. 17.00
Till innehållsförteckningen för Referensmetodik: Tarminfektioner, 2:a upplagan 2002
Speciell epidemiologi-infektioner i mage och tarm
Bakteriella infektioner
Salmonella (uppdaterad mars 2012)
Salmonella har global utbredning och förekommer hos en mängd olika djur utan symtom. Bakterierna sprids huvudsakligen via livsmedel. De är mycket resistenta mot kyla och uttorkning och kan tillväxa i födoämnen, även vid förhållandevis låga temperaturer, men de överlever inte temperaturer över +70°C. Bakterierna sprids med livsmedel, vatten och miljö samt mellan människor och via direktkontakt med djur.
Sverige har en lång historia av bekämpning av Salmonella i hela smittspridningskedjan från foder till livsmedel och människa. Nuvarande övervakning och kontroll fastlades i samband med Sveriges EU-inträde vilket också ger Sverige så kallade salmonellagarantier det vill säga rätt att ha särskilda krav vid införsel av vissa djur och livsmedel. Som en följd av Sveriges helhetssyn på salmonellabekämpning är salmonellasituationen hos människa unik i ett internationellt perspektiv med i princip salmonellafria svenskproducerade livsmedel och en majoritet av fallen smittade utomlands. I de flesta andra europeiska länder är situationen den omvända med flest fall smittade inom det egna landet. I Sverige rapporteras 3000-4000 fall årligen och även om cirka 80 % är smittade utomlands utgör ändå det stora antalet en icke försumbar sjukdoms- och samhällsbörda. Bärarfrekvensen av Salmonella bland friska personer i industriländer har uppskattats till 0,1 % - 0,2 %.
Som ett resultat av det omfattande kontrollprogrammet ligger den inhemska incidensen av Salmonella stabilt mellan 5-10 fall per 100 000 invånare. Mindre variationer ses mellan åren vilket beror på att antalet inhemskt smittade fall varierar med hur många utbrott det har varit.
Antalet utlandssmittade fall har minskat sedan början av 2000-talet. Denna trend håller i sig och 2011 var antalet utlandssmittade fall (2072, 73 %) det lägsta sedan början på 1980-talet. Tar man hänsyn till det genom åren ökade antalet utlandsresor blir minskningen ännu tydligare. Den största minskningen av fall har skett i europeiska länder där Spanien är det främsta exemplet. Spanien var tidigare det vanligaste smittlandet för Salmonella och trots att det är ett av svenskarnas vanligaste resmål så har risken att smittas av Salmonella sjunkit drastiskt under 2000-talet. Ett antal åtgärder inom EU för att kontrollera Salmonella inom fjäderfänäringen har gett resultat också i övriga Europa. Mellan 2004-2009 nästan halverades antalet rapporterade salmonellafall inom EU.
Cirka hälften av salmonellafallen är vuxna i åldern 30-69 år och i resten av åldersgrupperna är fallen relativt jämnt fördelade. En knapp fjärdedel av fallen är barn och ungdomar under 20 år (data från 2011).
Inhemska fall anmäls med en tydlig säsongsvariation med flest fall i juli och augusti. Flest utlandssmittade fall anmäls däremot under de månader då flest svenskar åker utomlands till varmare resmål det vill säga i januari till mars. De tre vanligaste serotyperna är S. Typhimurium, S. Enteritidis (19 %) och monofasisk Typhimurium (4,[5], 12:i:-). dis och S. Typhimurium. Detta speglar Sveriges unika läge med färre fall av inhemsk Salmonella och där Typhimurium är vanligaste serotypen, medan det internationellt sett är Enteritidis som är vanligast.
Djurbesättningar och livsmedel av animalt ursprung har i Sverige idag en, internationellt sett, unikt låg förekomst av Salmonella. Stora ansträngningar bör göras för att upprätthålla den mycket låga nivån (<0,1 %) Salmonella i råvaror och slaktdjur. Målsättningen är att såväl inhemskt producerade som importerade livsmedel ska vara fria från Salmonella. Ett tiotal salmonellautbrott utreds årligen. Misstänkt smittkälla är vanligen importerade livsmedel. Genom åren har ett skifte setts från animaliska smittkällor till vegetabiliska smittkällor som groddar och sallat.
Tyfoid- och paratyfoidfeber
S. Typhi och S. Paratyphi har endast människa som reservoar. De rapporterade fallen av tyfoidfeber har varit ganska konstant under många år. Under 1999 noterades ett utbrott av paratyfoidfeber i den turkiska turistorten Alanya då 305 europeiska turister smittades varav 80 svenskar. De inhemska fall som inträffat har varit sekundärfall eller laboratoriesmitta. Den senaste tio-årsperioden (2002-2011) rapporterades cirka 10 - 30 fall/år, praktisk taget alla smittade utomlands. Ett undantag var ett mindre utbrott med paratyfoid i Skåne 2007 som drabbade 16 personer.
Två olika vacciner mot tyfoid finns. Ett levande attenuerat och ett innehållande Vi-antigen.
Shigella (uppdaterad mars 2012)
Shigella har människa som huvudsaklig reservoar. Den låga infektionsdosen medför stor smittsamhet inte bara genom livsmedel och vatten utan också från person till person.
Cirka 400-699 fall av shigellainfektion rapporteras årligen till Smittskyddsinstitutet. De inhemskt rapporterade fallen utgör normalt 80-85 % och varierar med antalet utbrottsfall för respektive år. De utbrott av inhemsk Shigella som har skett i Sverige har framförallt berört förskolor mycket på grund av att bakterien sprids väldigt lätt mellan personer i den miljön. Även livsmedelsburna utbrott har inträffat. De utlandssmittade fallen varierar med svenskars resvanor. Av de inhemska fallen syns en tydlig topp under september och oktober, beroende på sekundär smittspridning på daghem från barn som smittats utomlands. Utlandsfallen var som flest i januari till mars då flest svenskar reser till varmare länder.
I Sverige är utbrott av Shigella inte vanliga. De utbrott som inträffar härleds ofta till att infekterade personer har hanterat mat som sedan ätits av andra. Det senaste livsmedelsburna utbrottet, där smittkälla kunde bekräftas, inträffade 2009 då cirka 50 personer insjuknade med Shigella dysenteriae typ 2 efter att ha ätit kontaminerade sockerärtor från Kenya. Drygt 140 personer insjuknade i ett stort utbrott 2008 efter att ha ätit lunch i en personalrestaurang i Stockholm. En ovanlig typ av Shigella sonnei konstaterades hos cirka hälften av fallen. En kohortstudie pekade på en ökad risk associerad med att ha ätit rårivna morötter från salladsbuffén, detta kunde dock aldrig bekräftas via odling och spårning av morötternas ursprung.
Årligen sker utbrott på förskolor där barn som varit magsjuka vistats och då smittat andra barn, syskon, föräldrar och personal. Dessa utbrott visar på vikten av att infekterade personer ska stanna hemma tills de inte längre utsöndrar bakterien. Under 1994 orsakade spansk importerad isbergssallad ett utbrott av shigellainfektion i landet med 50 rapporterade fall. Även andra länder i Europa fick shigellautbrott orsakade av denna isbergssallad. I västvärlden dominerar infektioner med Shigella sonnei som oftast ger relativt mild sjukdom. De allvarligaste dysenterifallen orsakas av Shigella dysenteriae typ 1 (Shiga´s bacill).
Så länge bakterien kan påvisas i feces är patienten smittsam. Risken för smitta är dock störst i det akuta skedet. Efter 3 veckor är 50 % smittfria utan behandling. Man bör vara generös med antibiotikabehandling vid shigellainfektion eftersom sjukdomsförloppet härigenom förkortas. Personer med riskyrke samt förskolebarn bör behandlas omgående av epidemiologiska skäl.
Smittbärare med riskyrke får inte utföra sitt normala arbete. Förskolebarn som är smittbärare får inte vistas på daghem. Som riskverksamhet betraktas yrkesmässig beredning eller hantering av oförpackade livsmedel liksom yrkesmässig vård av spädbarn eller patienter med nedsatt immunförsvar.
Yersinia (uppdaterad april 2012)
Yersiniainfektion är en zoonos, vilket innebär att den kan överföras mellan djur och människa. Sjukdom hos människa orsakas av arterna Y. enterocolitica eller Y. pseudotuberculosis. Perioden 2002-2011 anmäldes till SMI årligen mellan 281-812 fall.
En analys av tillgängliga mikrobiologiska data (Sminet) hos fall som rapporterats under åren 2007-2011 visade att Y. enterocolitica var vanligast i Sverige liksom i övriga Europa. Av 2141(84,5 %) fall hade 1809 fall infekterats med Y. enterocolitica, 11 (0,5 %) fall med Y. pseudotuberculosis, medan övriga 321 (15 %) fall saknade uppgift om art, vilken kan antas bestå av annan art av Yersinia men sannolikt också av Y. enterocolitica.
De rapporterade fallen (2007-2011) av Y. enterocolitica fördelade sig på de för Europa mest relevanta serogrupperna enligt följande: 1135 fall (63 %) med O3, 178 (10 %) med O9, 9 fall med O5, 27 samt 2 fall med O8. Intressant är de ovanliga fynden av O8 där båda fallen smittats inom landet. Denna serotyp är vanligen kopplad till den mest virulenta biotypen, 1B. Biotyp 1B återfinns mest i nya världen och i framför allt USA dominerar serogrupp O8 inom denna biotyp. Uppgift om biotyp bland de svenska fynden av O8 saknas dock, eftersom fullständig biotypning inte utförs i Sverige. I de återstående 27 % av fallen saknas uppgift om serotyp. Bland dessa återfinns 22 fall av den icke patogena biotypen 1A, som f.n. inte rapporteras separat i Sverige. Biotyp 1A är den vanligaste biotypen i de länder, t.ex. Finland, som utför analysen och rapporterar fynden.
Yersinia sprids sannolikt via förorenat vatten eller livsmedel och fläskkött är troligen det vanligaste livsmedlet för överföring av smittan till människa. De flesta av de som rapporteras med yersiniainfektion smittas i Sverige, cirka 75 % av alla fall årligen. Majoriteten av fallen är små barn och åldergruppen 0-4 år motsvarar omkring 30 % av de inhemska fallen.
En trendanalys av de inhemska fallen mellan 2004-2011 gjordes på samtliga fall men också på barn yngre än 1 år och barn i åldrarna 1-6 år. För alla undersökta åldersgrupper sågs en statistiskt signifikant nedåtgående trend utom för barn under 1 år. Den nedåtgående trenden i övriga grupper var signifikant på 5 % -nivån både med quasipoissonmodellen och med chi2-test för trend.
Campylobacter (uppdaterad mars 2012)
Campylobacterinfektion är den vanligaste orsaken till bakteriell gastroenterit i Sverige. Sjukdomen är en zoonos d v s den kan överföras mellan djur och människor. Fåglar är en naturlig reservoar men även andra djur som gris, nötkreatur, får och getter kan utsöndra bakterien via avföring. Vanligt förekommande smittvägar är otillräckligt tillagad kyckling och opastöriserad mjölk . Förorening med Campylobacter är en vanlig orsak till vattenburna utbrott. Infektion med Campylobacter orsakas hos människa oftast av arterna C. jejuni och C. coli. Totalt rapporterades i Sverige årligen drygt 8000 fall under 2010 och 2011. De flesta fallen rapporteras smittade utomlands, närmare 60 %. Inhemsk smitta sker framförallt under sommarmånaderna. Mellan 1998-2011 sågs ingen signifikant trend i antalet inhemska fall.
EHEC-Enterohemorragiska Escherichia coli (uppdaterad mars 2012)
Infektion med enterohemorragisk E.coli (EHEC) är en zoonotisk sjukdom som kan ge allvarlig sjukdom hos människa. Framförallt drabbas små barn. Sjukdomen kan ge blodig diarré och leda till komplikationen hemolytiskt uremiskt syndrom (HUS). Dödsfall förekommer. Nötkreatur är den huvudsakliga reservoaren för de shigatoxinproducerande bakterierna. Människor smittas via kontaminerade livsmedel, vatten och miljö eller vid direktkontakt med djur eller mellan människor. Sedan den 1 januari 1996 ingår EHEC O157 bland de smittsamma sjukdomar som skall anmälas enligt smittskyddslagen och sedan 1 juli 2004 är alla serotyper anmälningspliktiga.
Sedan 2005 då det största EHEC-utbrottet i svensk historia inträffade, det så kallade "salladsutbrottet", har flera åtgärder vidtagits på myndighetsnivå för att bekämpa och förebygga fall av EHEC på människor. En riskprofil och en myndighetsgemensam handlingspolicy finns för hantering av EHEC. Syftet med dessa båda dokument är att harmonisera myndigheternas arbete. Ett kontrollprogram för shiga(vero)toxinbildande E.coli hos nötkreatur är under uppbyggnad.
I Sverige rapporteras 200-300 fall årligen. Sedan alla serotyper blev anmälningspliktiga 2004 har det, med undantag av 2005 och salladsutbrottet, varit en minskande trend för den inhemska EHEC-incidensen som legat mellan 1-2 fall per 100 000 invånare. År 2010 bröts den trenden och incidensen ökade vilket höll i sig också 2011 med den högsta inhemska incidensen sedan utbrottsåret 2005. Andelen inhemsk smitta har under första hälften av 2000-talet legat på cirka två tredjedelar, medan denna andel har sjunkit under senare delen av 2000-talet för att ligga runt hälften de senaste åren.
Barn är överrepresenterade bland EHEC-fallen. Åldersgruppen 1-4 år är den vanligaste. Inhemska EHEC-fall rapporteras med en tydlig säsongsvariation med fler fall under sommarmånaderna.
Stora EHEC-utbrott är ovanliga i Sverige och majoriteten av fallen är sporadiska. Ett fåtal mindre utbrott på dagis eller i familjekretsar inträffar årligen vilket beror av att EHEC är smittsamt och endast ett fåtal bakterier behövs för att orsaka sjukdom. Årligen utreds ett 10-tal misstänkta kopplingar till djur och gårdar och där den vanligaste smittvägen är direktkontakt med djur och dess gödsel, framförallt från nötkreatur eller får, eller att ha druckit opastöriserad mjölk. En fallkontrollstudie för att identifiera riskfaktorer för inhemska sporadiska fall av EHEC i Sverige utfördes vid SMI 2009-2011. Denna visade att riskfaktorer förknippade med smitta via miljön, som till exempel att ha druckit obehandlat vatten eller att någon i familjen arbetar med nötkreatur, är smittvägar som är minst lika viktiga som kontaminerade livsmedel.
Mellan maj till juli 2011 pågick i Tyskland det internationellt största och allvarligaste EHEC- och HUS-utbrottet med 3816 fall inklusive 845 HUS-fall och 54 dödsfall. Resenärer från ett flertal länder drabbades och Sverige rapporterade det högsta antalet fall (53) utanför Tyskland. Alla svenska fall utom ett kunde kopplas direkt till Tyskland genom resa eller kontakt med familjemedlem som rest i Tyskland. Av de 53 fallen utvecklade 18 (34 %) komplikationen HUS och ett fall avled. Andelen HUS var ovanligt hög både i Sverige och i Tyskland och detta allvarliga förlopp utmärker utbrottet. En annan anmärkningsvärd iakttagelse var att majoriteten av fallen var vuxna. Utbrottet orsakades av en enteroaggregativ verotoxinproducerande E.coli (EAEC) med typen O104:H4 och var således inte en vanlig EHEC. Bakterien var ESBL-producerande och var tidigare inte vanligt förekommande internationellt. I en omfattande utredning i Tyskland kunde smittkällan spåras till förtäring av groddar av bockhornsklöverfrön där fröna hade importerats från Egypten där kontaminationen troligen skett.
EHEC O157 är normalt sett den vanligaste serogruppen bland både inhemskt och utlandssmittade fall. Ett trendskifte noterades 2009 då gruppen icke-O157, som består av ett flertal olika serogrupper, blev vanligare än O157 bland inhemska EHEC-fall. Sedan dess har denna grupp blivit allt vanligare. Tysklandsutbrottet visade att det är viktigt att ha en beredskap även mot ovanliga EHEC-typer, något som görs rutinmässigt vid SMI, och inte bara följa de som redan är kända. Effektiv behandling mot EHEC saknas och man får inrikta sig på att behandla de komplikationer som uppstår. Antibiotikabehandling rekommenderas inte vid EHEC-infektion.
Kolera
Kolera är en huvudsakligen vattenburen smitta. Dess epidemiologi kännetecknas av explosiva utbrott som ofta startar i flera distinkta foci samtidigt och sprider sig över världen som pandemier, vilka kan fortgå i åratal. De sex första pandemierna har utgått från Gangesdeltat, den första 1817. Den sjunde stora pandemin av typ O1 El Tor, började 1961 i Indonesien och nådde Peru i Sydamerika 1991. Därefter uppträdde 1992, först i Indien sedan i Bangladesh, en ny serogrupp, O139 "Bengal" i epidemisk form.
Personer med akut kolera utsöndrar mellan Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://wikimedia.org/api/rest_v1/":): {\displaystyle 10^7} och Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://wikimedia.org/api/rest_v1/":): {\displaystyle 10^1} Misslyckades med att tolka (MathML med SVG- eller PNG-återgång (rekommenderas för moderna webbläsare och tillgänglighetsverktyg): Ogiltigt svar ("Math extension cannot connect to Restbase.") från server "https://wikimedia.org/api/rest_v1/":): {\displaystyle ^3} organismer per gram avföring. Många insjuknar inte alls eller endast med milda symtom och fungerar som reservoarer för vidare spridning. Kolerabakterier kan också kolonisera zooplankton och epidemier har kopplats samman med sådan blomning.
Infektion med klassisk V. cholerae medför immunitet medan skyddet efter infektion med biotyp El Tor är svagare.
Tillgängliga vaccin består av avdödade helcells/toxoid preparationer eller helcellsberedningar av levande försvagade stammar för oralt bruk.
Ett fåtal fall har rapporteras i Sverige under den senaste tioårsperioden. De flesta har smittats utomlands men fall av laboratoriesmitta har också förekommit.
Helicobacter pylori
Helicobacter pylori är en vanlig orsak till gastrit. I Skandinavien uppskattas 30-40 % av hela befolkningen vara infekterad och i vissa invandrargrupper är prevalensen ännu högre. Smitta sker ofta under barnaåren och i Nordeuropa förvärvar årligen ca 1 % av förskolebarnen H. pylori-infektion. På grund av bättre levnadsförhållanden har incidensen minskat under de senaste decennierna och den kommer sannolikt att fortsätta minska. Det finns inga reservoarer för H. pylori påvisade utanför människa. (Information från Läkemedelsverket 1996; 7:23).
Clostridium difficile
Clostridium difficile förekommer sannolikt i den normala tarmfloran hos de flesta människor, dock oftast i så små mängder att speciella anrikningsmetoder måste användas för att kunna påvisa den. Med rutinmetoder kan C. difficile påvisas hos endast 2-4 % av friska vuxna, jämfört med cirka 70 % av spädbarn (< 1år) hos vilka bakterien ofta förekommer i stora mängder. Signifikansen av att påvisa C. difficile hos små barn är därför tveksam. I motsats till förhållandet hos vuxna, förefaller intestinaltrakten hos små barn dessutom i de flesta fall vara opåverkbar av C. difficile-toxin, även om fall av pseudomembranös kolit (PMC) i späd ålder finns beskrivna. Asymtomatiskt bärarskap förekommer, framför allt hos äldre sjukhusvårdade patienter.
Fall av C. difficile-medierad sjukdom är ett nosokomialt problem som har ökat under de senaste åren. Om detta är resultat av ökad antibiotikaanvändning, sämre vårdhygien, en utökad laboratoriediagnostik, eller en kombination av flera faktorer är oklart. Organismen är i Sverige idag den vanligaste orsaken till inhemsk bakteriell diarré (> 5 000 fall/år) och även den vanligaste orsaken till nosokomial bakteriell diarré. Vid PMC, som är den minst vanliga formen av C. difficile-sjukdom, är mortaliteten ca 20 %.
Antibiotikabehandling är den i särklass viktigaste riskfaktorn när det gäller C. difficile-diarré. Cirka 30 % av antibiotikaassocierad kolit/diarré orsakas av C. difficile. Andra predisponerande faktorer är hög ålder, (flertalet patienter är över 64 år), underliggande sjukdom, t.ex. malignitet, njurinsufficiens, sjukhusvistelse, tarmkirurgi, ventrikelsond och cytostatikaterapi. Vid de svåra kolitfallen föreligger oftast flera av riskfaktorerna samtidigt.
Bakteriell resistensutveckling
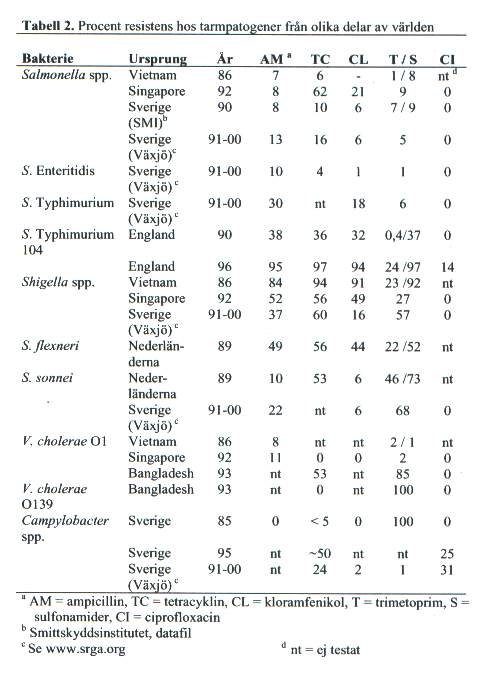
Av de antibiotika som kommit till användning vid tarminfektioner har resistens mot ampicillin, kloramfenikol, trimetoprim sulfa och kinoloner särskilt uppmärksammats [Tabell 2]. Resistensgenerna är ofta plasmidmedierade och uppträder tillsammans. De bakterier som bär tre eller fler olika resistensgener benämns multiresistenta. Hos Salmonella species och Shigella species är multiresistenta stammar ett vanligt och ökande fenomen, särskilt i utvecklingsländer men även i den industrialiserade delen av världen. Den senaste utvecklingen hos non typhi Salmonella-bakterier gäller multiresistenta isolat som dessutom förvärvat resistens mot kinoloner, trots att kinolonresistens ännu ej visats vara överförbar. Rapporter från England beskriver detta som ett problem hos både djur och människa, särskilt som de resistenta stammarna också tycks vara mer virulenta. Campylobacter är en annan tarmpatogen där resistens mot kinoloner ökat snabbt under senare år, sannolikt på grund av det i många länder utbredda bruket av kinoloner vid uppfödning av kyckling. Orsaken till kinolonresistens hos Campylobacter species är densamma som hos andra bakterier, nämligen en mutation i genen som kodar för enzymet DNA gyras, vilket är angreppspunkten för kinoloner. Hos Vibrio cholerae O1 har resistens mot flera av ovan nämnda antibiotika påträffats. I den senast beskrivna epidemin i Sydöstasien av V. cholerae O139 visade sig resistens mot trimetoprim/sulfa och streptomycin vara överförbar via ett genetiskt element som integrerats i kromosomen. Diarré orsakad av toxinbildande Clostridium difficile är ett exempel på störningar i tarmfloran som följd av antibiotikaanvändning. Clostridium difficile är en bakterie som är naturligt resistent mot många antibiotika och som därmed har en överlevnadsfördel vid långvarig antibiotikabehandling
Parasitinfektioner
Blastocystis hominis
Smittvägen har ej kunnat bevisas experimentellt men B. hominis överförs troligen den fekala-orala vägen. B. hominis är en vanligt förekommande organism världen över, så även i Sverige, där en daghemsstudie visade på en hög prevalens (7 av 51 barn) oavsett tidigare utlandsvistelse (Lebbad et. al.). Sambandet med gastrointestinala infektioner har ifrågasatts. Blastocystis spp. finns beskrivna hos en mängd olika djurarter men det är ej klarlagt om dessa organismer är B. hominis eller andra species.
Balantidium coli
Smittan överförs direkt genom fekal-oral kontakt via händer infekterade med cystor från svinfeces eller genom intag av kontaminerad föda eller förorenat vatten. Infektion hos människa är ovanlig och förekommer mest i varmt klimat i områden med låg hygienisk standard. I industrialiserade länder med kallare klimat är svinuppfödare och veterinärer riskgrupper. Epidemisk spridning mellan människor kan etablera sig om låg personlig hygien föreligger.
Cryptosporidium parvum
Cryptosporidium-oocystor är mycket motståndskraftiga mot olika desinfektionsmedel och kan liksom Giardia-cystor överleva i klorerat dricksvatten. De vanligaste smittvägarna är kontakt med infekterade djur, person till person smitta eller via infekterat vatten eller genom föda. Cryptosporidium parvum förekommer globalt, men är vanligast i områden med dålig omgivningshygien. Undersökning av råvatten till svenska reningsverk visade att 32 % av proverna innehöll misstänkta Cryptosporidium-oocystor. Varje år rapporteras mellan 30 -100 fall av kryptosporidios till SMI.
Cyclospora cayetanensis
Infekterade personer utsöndrar osporulerade (ej infektiösa) oocystor med feces, vilket gör person till person smitta osannolik. Oocystorna sporulerar efter en till två veckor och smittan överförs indirekt via kontaminerad föda eller genom vatten. Det finns ingen känd djurreservoar för Cyclospora. Sedan mitten av 1980-talet har Cyclospora förekomst rapporterats från de flesta delar av världen. I USA har utbrott rapporterats i samband med konsumtion av hallon och basilika.
Dientamoeba fragilis
Troligaste smittväg är fekal-oral smitta, något som dock ifrågasatts då känt cyststadium saknas och trofozoiten snabbt förstörs utanför kroppen. Transmission via Enterobius vermicularis (springmask) ägg infekterade med Dientamoeba fragilis har också föreslagits. Utbredningen är global. En studie från ett barnsjukhus i Kanada visar att D. fragilis var det vanligaste parasitfyndet under en femårsperiod. En svensk daghemsstudie visade att Dientamoeba fragilis var en vanligt förekommande parasit med 8/51 barn infekterade (Lebbad 1998).
Entamoeba histolytica
Människa är den enda reservoaren för Entamoeba histolytica. Cystor av E. histolytica sprids via vatten eller föda. Cystorna överlever klorering men avlägsnas vanligtvis från dricksvattnet med sandfiltrering.
E. histolytica förekommer i hela världen, men är endast endemisk i områden med dålig omgivningshygien. Av världspopulationen beräknas 3-10 % vara infekterade. Enligt en WHO-rapport från 1998 orsakar amöbainfektion ca 70 000 dödsfall om året. Av protozoinfektionerna är amöbiasis den fjärde ledande dödsorsaken efter malaria, Chagas´ sjukdom och leishmaniasis.
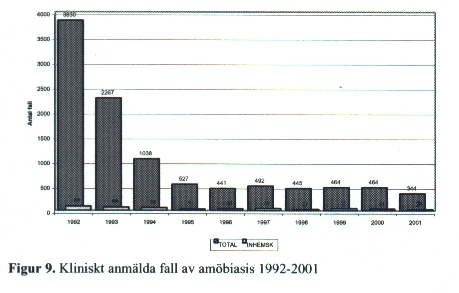
År 2001 anmäldes 344 fall av Entamoeba histolytica till SMI men 90-95 % av dessa är antagligen E. dispar, se vidare i speciell del. Endast ett fåtal av dessa har smittats inom landet och det är främst sekundärfall till utlandssmittade men även sexuell smittöverföring rapporteras. Toppen 1992 – 93 återspeglar ett stort antal asylsökande [Fig. 9].
Giardia intestinalis
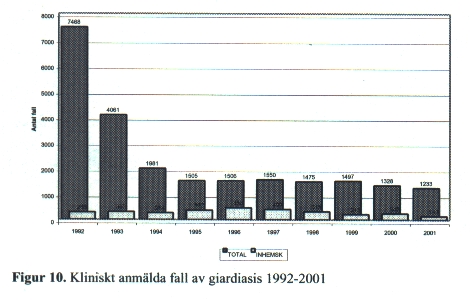
Cystorna är mycket motståndskraftiga mot olika desinfektionsmedel och kan överleva i klorerat dricksvatten. Smittan överförs via intag av vattenburna cystor eller genom direkt kontakt med en infekterad person. Morfologiskt identiska parasiter finns hos husdjur och vilda däggdjur men transmission mellan djur och människa är ännu inte fastställd och det är ovisst om Giardia från djur kan smitta en människa. Giardia-infektion förekommer endemiskt i områden med låg hygienisk standard, sprider sig mellan barn på daghem och är vanlig hos resenärer. Den kan också förekomma i vattenburna utbrott efter avloppsförorening av kommunalt dricksvatten. De senaste fyra åren har cirka 1 400 kliniska fall/år rapporterats till SMI [Fig. 10]. Av dessa har majoriteten smittats utomlands. De inhemska fallen beror till stor del på smittspridning bland barn på daghem.
Isospora belli
Infekterade individer utsöndrar oocystor med feces. I motsats till Cryptosporidium är oocystorna ej infektiösa omedelbart efter utsöndring vilket gör person till person smitta sällsynt. Sporuleringen tar ett till två dygn och resulterar i mogna infektiösa oocystor med två sporocystor. Dessa för smittan vidare via infekterad föda eller vatten. Isospora belli förekommer främst i tropiska och subtropiska delar av världen och är endemisk i delar av Sydamerika, Afrika och Sydostasien.
Microsporidia
Innan 1985, då Enterozytozoon bieneusi beskrevs första gången var endast en handfull fall av human mikrosporidia-infektion rapporterade. Sedan dess har mikrosporidiafall beskrivits från i stort sett hela världen inklusive Sverige (Svedhem 1998), de flesta i form av E. bieneusi-infektioner hos aids-patienter. Introduktionen av antiviral behandling har resulterat i ett kraftigt minskat antal fall av aids-relaterad mikrosporidia-infektion (Conteas 1998). Mikrosporidios orsakad av såväl E. bieneusi som E. intestinalis har också upptäckts i enstaka fall hos immunkompetenta individer, då i samband med självläkande diarré (Svenungsson 1998). Inget fynd av microsporidia ingick i den frivilliga laboratorierapporteringen 1998-2000.
Virusinfektioner
I Sverige uppträder diarrésjukdomar orsakade av rotavirus, calicivirus och astrovirus huvudsakligen under vinterhalvåret medan infektioner orsakade av adenovirus förekommer året runt. Upp till 10e9–10e10 viruspartiklar utsöndras i kräkningar och i feces hos akut sjuka patienter samtidigt som den dos som orsakar sjukdom beräknas vara så låg som 10-100 partiklar, vilket förklarar den mycket snabba spridning som kan ses på daghem, i skolor, på sjukhusavdelningar och andra institutioner som vårdar patienter. Generellt utsöndras virus i feces så länge gastrointestinala symtom föreligger, vilket aktualiserar kravet på relevant provtagning. Fecesprov för virus/virusantigen påvisning skall tas när patienten har symtom. Smittspridningen är fekal-oral. Samtliga virus som orsakar gastrointestinala symtom är mycket motståndskraftiga mot olika desinfektionsmedel och infektiösa partiklar kan överleva 1-2 veckor på ytor som ett dörrhandtag eller leksaker i ett väntrum på en barnavdelning.
Rotavirus
Rotavirus är den vanligast förekommande patogenen hos yngre barn med akut gastroenterit. Nosokomiala infektioner med rotavirus är vanliga på barn- och geriatriska avdelningar. I Sverige uppträder diarrésjukdomar orsakade av rotavirus huvudsakligen under vinterhalvåret. Rotavirus indelas i undergrupper och grupperna A-C har identifierats hos människa.
Grupp A rotavirus är den vanligast förekommande undergruppen. Mellan 1500-1700 barn sjukhusvårdas årligen i landet p.g.a. en akut rotavirus grupp A infektion. Rotavirus grupp A infektioner är också associerade med en signifikant mortalitet främst i u-länder där ca 600 000 dödsfall inträffar per år. Enstaka dödsfall förekommer även i Sverige.
Grupp B rotavirus har hittills endast påvisats i Kina och Indien.
Grupp C rotavirus har isolerats i Sverige och har i en svensk prospektiv undersökning bland vuxna med diarrésjukdom visats förekomma hos 1/3 av de 3 % som med elektronmikroskopi visades utsöndra rotavirus.
Flera vacciner mot rotavirus grupp A infektioner har prövats med varierande resultat. Kliniska prövningar pågår för närvarande med åtminstone två tänkbara orala attenuerade vaccinkandidater, en genrekombinerad bovin rotavirusstam och en human rotavirus stam av serotyp 1. Lovande resultat i fas 2 prövningar före¬ligger.
Calicivirus
Calicivirus är den viktigaste orsaken till nosokomiala och födoämnesburna diarréutbrott i Sverige. Ca 200 diarréutbrott/år diagnostiseras vid SMI med hjälp av elektronmikroskopi. En majoritet av dessa utbrott visar sig vara utlösta av calicivirus tillhörande gruppen Norwalk-liknande virus. De diarréutbrott som uppträder på sjukhus resulterar i stora praktiska vårdproblem med stängningar av vårdavdelningar och orsakar därmed höga samhällskostnader. Calicivirus drabbar individer i alla åldrar. Calicivirus kan påvisas i kontaminerat vatten, frusna bär, bageriprodukter, sallad och skaldjur. Infektioner med calicivirus uppträder främst under vinterhalvåret.
Astrovirus
Astrovirus orsakar gastroenterit främst hos yngre barn men även institutionsvårdade äldre individer. Astrovirus är orsaken i 1-6 % av barn inlagda med en akut diarrésjukdom. Astrovirus kan förorsaka såväl epidemiska utbrott som sporadiska fall. Ett flertal internationella epidemiologiska studier visar att antikroppar riktade mot astrovirus uppträder tidigt i barndomen och vid 5 års ålder har ~70 % av barnen antikroppar mot astrovirus. Inga svenska studier föreligger. Astrovirus infektioner uppträder främst under vinterhalvåret.
Enteriska adenovirus
Adenovirus 40 och 41 har i Sverige identifierats hos sjukhusvårdade barn med diarrésjukdom i en frekvens av 8 % och i olika internationella studier 4-15 %. Vid tre års ålder har 30-100 % av barn neutraliserande antikroppar riktade mot adenovirus 40 och 41. Adenovirus infektioner förekommer endemiskt året om.
REFERENSER
- Lebbad M, Nääs J, Tjernström K. Parasiter på daghem. Svenska Läkarsällskapets Riksstämma, 24-26 november 1998, Göteborg.
- Conteas C N, Berlin O G, Speck C E, Pandhumas S S, Lariviere M J, Fu C. Modification of the clinical course of intestinal microsporidiosis in acquired immunodeficiency syndrome patients by immune status and antihuman immunodeficiency virus therapy. Am J Trop Med Hyg 1998;58:555-558.
- Smittsamma sjukdomar 2001. Årsrapport från avdelningen för epidemiologi. SMI tryck 136-2002
- Svedhem V, Lebbad M, Struve J, Veress B, Andström E, Aust-Kettis A, Linder E. Microsporidia in duodenal biopsies from 72 HIV-infected patients with abdominal complaints. APMIS 1998;106:535-538.
- Svenungsson B, Capraru T, Evengard B, Larsson R, Lebbad M. Intestinal microsporidiosis in a HIV-seronegative patient. Scand J Infect Dis 1998;30:314-316.