Skillnad mellan versioner av "Intraabdominella infektioner"
| Rad 128: | Rad 128: | ||
'''Diagnos''': Tecken på infektion i efterförloppet till pankreatit är feber och ospecifika buksmärtor/ömhet samt allmänpåverkan. Labdata inklusive serumamylas och LPK är ospecifika medan CRP-stegring har högre specificitet. | '''Diagnos''': Tecken på infektion i efterförloppet till pankreatit är feber och ospecifika buksmärtor/ömhet samt allmänpåverkan. Labdata inklusive serumamylas och LPK är ospecifika medan CRP-stegring har högre specificitet. | ||
| − | '''Diagnosen''' ställs med datortomografi medan ultraljud har begränsat värde. Intravenös kontrasttillförsel kan vid datortomografi visualisera ischemiska områden där chansen att finna infekterat material med finnålsbiopsi är störst. Infektionskomplikation efter pan-kreatit är en terapeutisk utmaning och det finns kirurgkliniker som är | + | '''Diagnosen''' ställs med datortomografi medan ultraljud har begränsat värde. Intravenös kontrasttillförsel kan vid datortomografi visualisera ischemiska områden där chansen att finna infekterat material med finnålsbiopsi är störst. Infektionskomplikation efter pan-kreatit är en terapeutisk utmaning och det finns kirurgkliniker som är superspecialiserade på strategier för omhändertagande av dessa mycket svårt sjuka patienter. |
| − | Bakteriefloran är ofta polymikrobiell och utgår från tarmen, sannolikt genom s.k. translokation till blodet. Total parenteral nutrition är nödvändig i det akuta skedet av pankreatit men predisponerar för sådan translokation. Enterobacteriaceae spp och enterokocker dominerar men även stafylokocker är vanliga agens. Nonfermentativa gramnegativa stavar och streptokocker förekommer mindre ofta och ovanliga agens är anaerober (''Bacteroides fragilis''), ''Haemophilus parainfluenzae'', ''Eikenella corrodens'' och jästsvamp. | + | Bakteriefloran är ofta polymikrobiell och utgår från tarmen, sannolikt genom s.k. translokation till blodet. Total parenteral nutrition är nödvändig i det akuta skedet av pankreatit men predisponerar för sådan translokation. ''Enterobacteriaceae'' spp och enterokocker dominerar men även stafylokocker är vanliga agens. Nonfermentativa gramnegativa stavar och streptokocker förekommer mindre ofta och ovanliga agens är anaerober (''Bacteroides fragilis''), ''Haemophilus parainfluenzae'', ''Eikenella corrodens'' och jästsvamp. |
| − | |||
==== Mjältabscess (D73.3) ==== | ==== Mjältabscess (D73.3) ==== | ||
Versionen från 17 november 2009 kl. 09.51
Till innehållsförtecningen för Referensmetodik: Bakteriologisk diagnostik av infektioner i hud, mjukdelar, skelett och inre organ
Intraabdominella infektioner
Peritonit (K65.0)
Peritonit är en inflammation i bukhålan som i regel är associerad med en bakteriell komponent. Det är mycket svårt att experimentellt framställa infektioner i fri bukhåla med enbart bakterier eftersom den stora peritonealytan har en suverän förmåga att opsonisera, fagocytera, destruera och transportera bort främmande material. För infektion krävs samtidig närvaro av vävnadskada eller toxiskt adjuvans såsom magsaft eller galla.
Primär peritonit (K67.-*)
är en infektion i bukhålan som inte föregås av en vävnadsdestruktion. Tillståndet är ovanligt. Hos kvinnor kan uppåtstigande infektioner via tuborna ge primär peritonit. Bakterier som normalt associeras med infektioner i luftvägarna, exempelvis pneumokocker, Haemophilus influenzae och S. pyogenes (GAS) samt meningokocker kan ta sig denna väg, men även den hematogena spridningsvägen är möjlig. Organ som kan drabbas av primär peritonit är appendix och inre genitalia. Gonokocker och Chlamydia trachomatis har isolerats vid perihepatit. Yersinia enterocolitica ger ibland en peritonitbild med symtom som vid akut appendicit, men där laparotomi eller laparoskopisk undersökning visar s.k. körtelbuk. Tuberkulös peritonit är vanlig i tredje världen, men utgör ett växande problem också i I-länder med hög AIDS-prevalens.
Hos AIDS-patienter och personer som missbrukat anabola steroider kan infektion med Bartonella spp ge s.k. peliosis hepatis, en sjukdom i levern och andra parenkymatösa organ som genom tillväxt av kärlendotel ger lakuner av vätska i nybildade hålrum.
Sekundär peritonit (K65.0)
Ursprunget till intraabdominella infektioner är nästan alltid en vävnadsskada som progredierar i närvaro av bakterier med ursprung från gastrointestinalkanalen. 3/4 av alla peritoniter beror på spontana perforationer av magtarmkanalen och 1/4 är komplikationer efter kirurgiskt ingrepp. Beroende på vävnadsskadans orsak och storlek (mekaniskt/kemiskt trauma eller vävnadsischemi p.g.a. kärlobstruktion) och tidsförloppet (successivt eller plötsligt massivt vävnadsgenombrott) uppstår en vätskeansamling och inflammation som är lokal eller diffus.
Under peritonitstadiet sker stora vätskeförluster från blodbanan. Toxiska metaboliter från vävnadsdestruktion respektive diverse bakteriella toxiner, framförallt endotoxin, tas upp i cirkulationen. Detta triggar via interleukiner den inflammatoriska försvarskaskaden till en gigantisk "brandkårsutryckning" som kan vara till men för patienten. Resultatet är ett livshotande ”septic inflammatory response syndrome” (SIRS) med chock, hypoxi och njurpåverkan och som fullt utvecklat ger en multiorgansvikt.
Bakterieflora: se Abscess nedan.
Tertiär peritonit
Patienter som p.g.a. dåligt immunstatus inte läker ut sin peritonit trots intensiv behandling kan övergå i en kronisk, persisterande atypisk diffus peritonit utan något säkert fokus. Bakteriefloran utgörs av KNS, Pseudomonas spp, svamp eller annan typisk nosokomial flora. Multiorgansvikt är vanlig och prognosen dålig.
Abscess (K65.0. ICD 10 kod beroende av primärlesionens lokalisation)
I bukhålan avgränsas det inflammatoriska infiltratet med fibrinutfällningar under loppet av några dagar/1 vecka till en abscess där den yttre avgränsningen slutligen organiseras till en kapsel. Innan abscessbildning ägt rum sker stora fysiologiska förändringar i bukhålan. Syrgastensionen är låg, CO2- och laktathalten hög medan peritonealinnehållet är extremt surt, pH 5,5-6,8; alltså förhållanden som avviker mycket kraftigt från laboratoriets standarder vid resistensbestämning.
Lokalisationen av en abscess bestäms av den primära skadan. Perforation av magsäck/tolvfingertarm var före introduktion av effektiv syrareducerande och helicobakterspecifik terapi, den vanligaste primärskadan. Den har nu minskat något i förhållande till perforationer på (i fallande ordning) appendix, tjocktarm, tunntarm och gallvägar. Gravitationen med tendens till sänkningsabscesser ned i lilla bäckenet (vanligaste abscesslokalen) motverkas av att främmande partiklar inklusive bakterier transporteras mot diafragmas undersida och bortförs via lymfatiska kanaler genom ett undertryck som uppstår vid andningsrörelser. Peritoneums speciella anatomi medger därigenom att t.o.m. dekliva skadelokaler, t.ex. appendix, kan dräneras uppåt med abscessbildning subfreniskt som följd. Andra abscesslokaler är subhepatiskt, parakoliskt, paracekalt och mellan tunntarmsslyngor.
Abscesser och infektioner i lever- och gallvägar, bukspottskörtel och mjälte beskrivs separat.
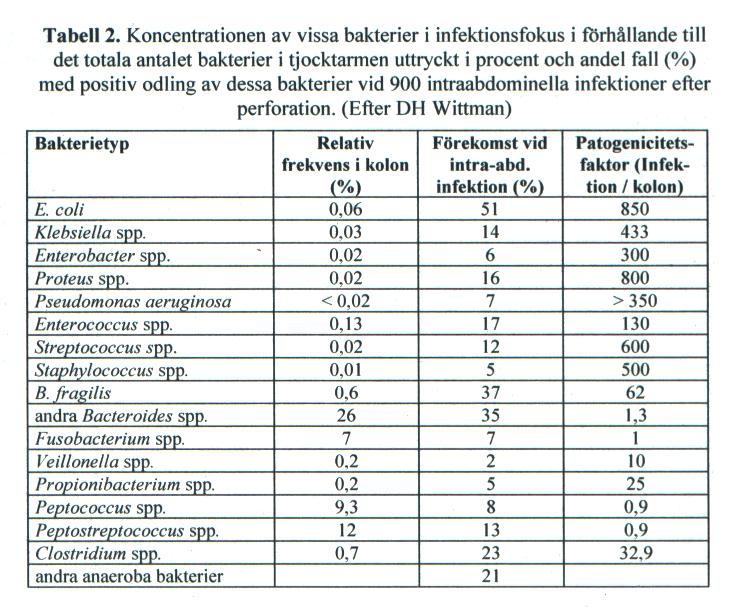
Bakteriefloran: Vid fekal peritonit kommer hela tarmfloran ut i fri bukhåla, men det sker redan inom några minuter en kraftig selektiv reduktion av florans samansättning. Eubacterium och Bifidobacterium spp, som finns i mycket stora koncentrationer i tarmen, decimeras snabbt till icke detekterbar nivå. Genom att jämföra den relativa koncentrationen i tarm av en viss stam mot dess relativa frekvens i infektionshärden hos ett stort antal patienter med peritonit, får man fram ett grovt mått på vilka arter som har resistens mot peritoneums avdödningsförmåga och därmed kandiderar som patogener under infektionsförloppet (se Tabell 2). Måttet är osäkert vid låg relativ frekvens i kolon.
Infektionsförloppet vid intraabdominell infektion är dynamiskt och bakteriefloran ändras över tiden. Ofta kan 5-10 olika arter isoleras med adekvat odlingsteknik. Processen beskrivs som en "mikrobiell progression" där aeroba stammar ( E. coli och enterokocker) dominerar i koncentration över anaerober (Bacteroides, Fusobacterium, Clostridium spp) under den septiska peritonitfasen, medan förhållandet är det motsatta under abscessfasen. Vid appendicit är Bilophila wadsworthia en viktig anaerob patogen.
Experimentella erfarenheter, vilka stöds av kliniska observationer, pekar på tydliga synergistiska effekter mellan aerober och anaerober i närvaro av toxisk adjuvans (gallsalter, bariumsulfat, steril feces):
- Monokultur av E. coli: sepsis, peritonit men ej abscess,
- Monokultur av enterokocker eller Bacteroides eller Fusobacterium spp: ej sepsis, ej peritonit, ej abscess (utom vissa stammar av kapselbärande B. fragilis),
- Blandkultur av E. coli och Bacteroides fragilis: sepsis, peritonit och abscess,
- Blandkultur av enterokocker och Bacteroides fragilis: ej sepsis, ej peritonit men abscess.
Endotoxin från E. coli och kapselsubstans från Bacteroides fragilis hos avdödade bakterier kan ge samma kliniska resultat som viabla bakterier.
Diagnostik: Diagnosen intraabdominell infektion kan i regel ställas enbart med anamnes och fysikalisk undersökning, t.ex. klassisk appendicit, men en icke obetydlig andel "akuta bukar" med inslag av infektion är svårtydbara. Datortomografi och ultraljud är till stor hjälp för att lokalisera och tömma infektionshärdar på pus via perkutan punktion/katetrisering.
Konklusion: Koch's postulat kan inte appliceras på intraabdominella infektioner eller på kirurgiska infektioner i allmänhet. Förloppet vid sekundär peritonit beror, utom i undantagsfall, mer på den ursprungliga vävnadsskadans lokalisation, omfattning och underliggande sjukdom samt andra patientrelaterade faktorer än vilka bakteriespecies som får tillträde.
CAPD-infektion eller PD-infektion (K 65.0)
CAPD (Chronic Ambulatory Peritoneal Dialysis) eller PD medger att den njursjuka patienten själv kan sköta sin dialys i hemmet. Via en speciell kateter genom hud och bukvägg kan dialysvätska tillföras peritonealhålan där bukhinnan fungerar som ett dialysmembran. Den vanligaste komplikationen är peritonit, vilket inträffar en gång per 20-60 patientmånader. Genom användning av slutna PD-system och implantation med 2-cuffs dialyskateter i bukväggen har peritonitfrekvensen reducerats. Recidiverande peritonit kan hos vissa patienter ge progredierande fibrösa adheranser, vilket förhindrar fortsatt CAPD och katetern måste avlägsnas.
Patogenes: Dialysvätskans låga pH och höga osmolaritet kan bidra till att reducera bakterieavdödningen intraperitonealt. Genom tillförseln av dialysvätska sker också en utspädning av opsoniner (IgG och C3), vilket minskar fagocyternas förmåga till avdödning.
Symtomen på CAPD-peritonit är smärta och ömhet i buken, ofta kombinerad med illamående, ibland feber och diarré. Dialysvätskan är grumlig med leukocytstegring (>100/mm3).
Infektionsvägar: Bakterier kan invadera via den tunnelerade inträdesporten, vilket är mindre vanligt, eller intraluminalt genom att kateterkoppling eller dialysvätska kontamineras. Andra möjliga inträdesportar är transmural migration av bakterier från tarm, s.k. translokation, eller genom hematogen insådd. I sällsynta fall med polymikrobiell tarmflora måste tarmperforation misstänkas. Candida spp kan hos kvinnor ge uppåtstigande infektion och peritonit via tuborna.
Bakterieflora: Hudbakterier är den vanligaste etiologin (Tabell 3) och domineras av KNS. En förklaring tros vara förmågan att kolonisera plastmaterial med en biofilm genom "ytkorrosion" och sedan producera ett slemskikt till skydd mot fagocyter. Den betydande resistensutvecklingen hos KNS mot antibiotika förstärks in vivo av bakteriernas tendens till minskad metabol aktivitet och celldelning.
Infektioner i gallvägar och lever
Anatomi
Galla produceras i levern och dräneras via höger respektive vänster levergång till den gemensamma levergången. Denna bildar tillsammans med gallblåsegången (ductus cysticus) den gemensamma gallgången (ductus choledochus), vilken i sin tur mynnar i tolvfingertarmen tillsammans med pankreasgången. Mynningen (Papilla vateri) omges av en kraftig sfinktermuskulatur som relaxeras på hormonella och nervösa impulser efter födointag. I gallblåsan lagras och koncentreras galla i väntan på sfinkterrelaxation. Hos den friska individen är galla fri från bakterier.
Stenbildning. Infektioner i gallvägarna hör nästan alltid ihop med avflödeshinder, framförallt stenbildning men även tumörer. Stenbildningen beror på imbalans i den kemiska sammansättningen av galla (gallsyror, fosfolipider och kolesterol). De vanligaste konkrementen är kolesterolstenar och blandstenar (kolesterol/pigment-/kalcium). Bakterier bedöms ha betydelse för bildningen av kalciumbilrubinatstenar. Det bakteriella enzymet betaglukuronidas (vanligt hos bl.a. E. coli) splittrar då konjugerat bilirubin från glukuronsyra så att fritt bilirubin kan binda kalk och bilda konkrement.
Riskfaktorer för bakteribili. Vid operation av gallblåsan i lugnt skede efter kolecystit är förekomsten av bakterier i galla (bakteribili) 15-30 %. Riskfaktorer för bakteribili är hög ålder, akuta operationer, gulsot, febertoppar under veckan före operation, operation inom 4 veckor efter en akut gallblåseinflammation (kolecystit), tidigare gallvägsoperation samt stenar eller annan obstruktion av gallflöde.
Akut kolecystit (K80.- och K81.-)
är en inflammation i gallblåsan som ger smärta och palpations- eller dunkömhet över höger revbensbåge samt illamående och ibland feber. Akut kolecystit är den gallvägsåkomma som oftast är associerad med infektion. I mer än 95 % av fallen orsakar ett ductus cysticus konkrement avflödeshinder från gallblåsan. Via tryckökning i gallblåseväggen induceras frisättning av prostaglandin som förhindrar absorption men ger vätskesekretion in i lumen med ytterligare tryckökning och en utspänd gallblåsa som följd.
I mer än 5 % föreligger akalkulös kolecystit, som uppkommer vid stora traumata, t.ex. olycksfall, operation eller brännskada. Gallblåsan tycks här vara ett chockorgan men patogenesen är ofullständigt känd.
Ungefär 3/4 av patienter med akut kolecystit har bakteribili med 10e5CFU/mL galla. Bakterieförekomst är starkt korrelerad med ökande ålder, gallblåsegangrän och feber (pos odling i 90 % om 38,5 oC). Patienter opererade inom 48 tim efter symtomdebut har den högsta frekvensen bakteribili.
Bakteriefloran domineras av E. coli, andra Enterobacteriaceae spp, enterokocker och streptokocker. Anaerober förekommer endast i ca 15 % med framförallt klostridier och andra grampositiva stavar samt kocker.
Vid akalkulös kolecystit ses en liknande flora men Staphylococcus aureus är vanligare liksom S. pyogenes (GAS) och Salmonella spp.
Postoperativa infektioner i operationsområdet (sårinfektion, abscess, peritonit) förekommer nu i 1-2 % och orsakas i regel av bakterier från gallvägarna. Bukväggsflegmone med Clostridium perfringens är en sällsynt men fruktad komplikation.
Kolangit (K80.3-K80.4-K83.0)
Avflödeshinder i andra delar av gallträdet än ductus cysticus ger tryckstegring upp i leverbädden och orsakar gulsot. Vid kolangit har patienten hög feber, smärta och ömhet i bukens övre högra del samt är allmänpåverkad. Gallan är nästan alltid infekterad och bakterier sprids i retrograd riktning ut i leverparenkymet med septikemi som följd. Sådan translokation av bakterier ut i blodbanan ger karaktäristiska temptoppar vid intermittent tryckstegring i gallvägar som inte är helt blockerade (ascenderande kolangit). Vid suppurativ kolangit föreligger total avstängning med pus under högt tryck, kontinuerlig bakteriemi och hög mortalitet.
Förutom konkrement och tumörer kan orsaken till kolangit vara iatrogen, exempelvis efter endoskopisk retrograd kolecystopankreaskopi (ERCP), där ickesterila endoskop kan inducera infektion.
Bakteriefloran påminner om den vid kolecystit, men det anaeroba inslaget är betydligt större. Bacteroides fragilis, som är en raritet vid kolecystit, och fusobakterier är vanligt förekommande. I fall med sjukhusakvirerad kolangit isoleras mer typisk nosokomial flora, exempelvis Pseudomonas, Proteus, Serratia spp, KNS och jästsvamp.
Leverabscess (K75.0)
Pyogen leverabscess kan förekomma solitärt eller multipelt (Entamoeba- och Eccinococcus-infektioner berörs inte här). Ursprungligt infektionsfokus är gallvägar (33 %), intraabdominellt (22 %), okänt (21 %), hematogent (13 %) och spridning per kontinuitatum, trauma samt metastas (11 %). Vid multipla abscesser dominerar gallvägsfokus stort. Underliggande sjukdomar är Mb Crohn och annan kronisk granulomatös sjukdom, diabetes, malignitet och AIDS.
Symtom: Leverabscess skall misstänkas vid långdragen trötthet, viktnedgång, aptitlöshet, anemi och låggradig feber. Mer alarmerande sjukdomsbilder förekommer med hög feber och septisk allmänpåverkan. Smärtor i buken kan vara diffusa men oftast lokaliserade till övre högra kvadranten med utstrålning till höger skulderblad.
Labprover visar förhöjda alkaliska fosfataser och lågt albuminvärde samt hög SR/CRP.
Diagnosen ställs med scintigram (technetium-, gallium-, indiummärkta leukocyter), ultraljud och datortomografi. Med ledning av de två sistnämnda läggs katetrar in perkutant för provtagning och dränage.
Bakterieflora: Den enskilt vanligaste patogenen är i moderna studier Streptococcus milleri-gruppen (Streptococcus constellatus, intermedius och anginosus). För övrigt påminner floran om den vid kolangit (E. coli, Klebsiella, Enterobacter, Proteus spp och enterokocker). Strikt anaeroba bakterier förekommer i ca hälften av fallen med Bacteroides, Fusobacterium och Peptostreptococcus spp. Polymikrobiell flora förekommer ofta med 2-4 stammar/prov. Ovanliga isolat är Listeria, Yersinia enterocolitica, Pasteurella multocida och Actinomyces spp. Hos barn är Staphylococcus aureus den viktigaste patogenen.
Infektioner i Pankreas (K85.9)
I <10 % av fall med bukspottkörtelinflammation (pankreatit) utvecklas en infektion i efterförloppet. I svåra fall uppträder infektionen i senare delen av det akuta inflammatoriska skedet, medan merparten kommer efter en latens på 2 3 veckor. Inflammationen kan åstadkomma ett okontrollerat frigörande av digestiva enzymer varvid större eller mindre delar av organet kan gå i nekros. Under förloppet svullnar pankreas, vilket ibland benämns "Pankreasflegmone". Efterhand utvecklas vätskefyllda hålrum med bl.a. blod och trögflytande nekrotiskt material, s.k. pseudocystor, som lätt koloniseras med bakterier. Resultatet blir en pankreasabscess som kan vara solitär eller multipel, i det senare fallet förkommer ibland inbördes kommunikation. Infekterad nekrotisk pankreasvävnad har en imponerande aggressiv förmåga att ge abscedering intraabdominellt, ned i lilla bäckenet och t.o.m. ut i mediastinum, pleura, bronker och halsregion samt penetrera huden.
Diagnos: Tecken på infektion i efterförloppet till pankreatit är feber och ospecifika buksmärtor/ömhet samt allmänpåverkan. Labdata inklusive serumamylas och LPK är ospecifika medan CRP-stegring har högre specificitet.
Diagnosen ställs med datortomografi medan ultraljud har begränsat värde. Intravenös kontrasttillförsel kan vid datortomografi visualisera ischemiska områden där chansen att finna infekterat material med finnålsbiopsi är störst. Infektionskomplikation efter pan-kreatit är en terapeutisk utmaning och det finns kirurgkliniker som är superspecialiserade på strategier för omhändertagande av dessa mycket svårt sjuka patienter.
Bakteriefloran är ofta polymikrobiell och utgår från tarmen, sannolikt genom s.k. translokation till blodet. Total parenteral nutrition är nödvändig i det akuta skedet av pankreatit men predisponerar för sådan translokation. Enterobacteriaceae spp och enterokocker dominerar men även stafylokocker är vanliga agens. Nonfermentativa gramnegativa stavar och streptokocker förekommer mindre ofta och ovanliga agens är anaerober (Bacteroides fragilis), Haemophilus parainfluenzae, Eikenella corrodens och jästsvamp.
Mjältabscess (D73.3)
Abscesser i mjälten är ovanliga men tycks öka något i frekvens. Solitära abscesser har bättre prognos än multipla; de senare antyder multiorganengagemang. Uppkomstmekanismen är i regel septiskt nedslag från något annat infektionsfokus, spridning per kontinuitatum från annat intraabdominellt infektionsfokus eller kolonisation av mjältinfarkt efter icke-penetrerande trauma. Den viktigaste infektionskällan är endokardit. Immundefekta patienter (diabetes, intravenöst missbruk, AIDS och cytostatikabehandling) löper större risk för mjältabscess.
Diagnos: Symtomen är ospecifika men nästan alla patienter har feber. Smärtor till vänster i övre delen av buken förekommer hos knappt hälften av fallen, emellanåt med utstrålning till vänster skuldra. Splenomegali ses i 50 %. Diagnosen ställs med ultraljud eller datortomografi. Scintigrafi har lägre känslighet.
Behandlingen är i regel splenektomi men vid solitära abscesser kan perkutant dränage ge utläkning.
Bakteriefloran är oftast aerob med dominans av Enterobacteriaceae spp, streptokocker (även mikroaerofila) och stafylokocker. Anaerober kan isoleras i ca 10 % (Bacteroides, Propionibacterium, Clostridium, och Fusobacterium spp). Candida-infektioner är ovanliga men viktiga att diagnostisera eftersom utläkning utan kirurgi kan ske tack vare moderna svampmedel.